
| A£® | ¢Ū¢Ü¢Ž | B£® | ¢Ś¢Ū¢Ż | C£® | ¢Ł¢Ś¢Ū¢Ż | D£® | ¢Ü¢Ž |
·ÖĪö Ė®ÖŠŌŖĖŲ»ÆŗĻ¼Ū¼Č²»ÉżøßŅ²²»½µµĶŹ±¼Č²»×÷Ńõ»Æ¼ĮÓÖ²»×÷»¹Ō¼Į£¬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗ¢Ł2Na+2H2O=2NaOH+H2”ü£¬Ė®ÖŠHŌŖĖŲ»ÆŗĻ¼ŪÓÉ+1¼Ū±äĪŖ0¼Ū£¬ŌņĖ®×÷Ńõ»Æ¼Į£»
¢Ś2H2O$\frac{\underline{\;µē½ā\;}}{\;}$2H2”ü+O2”ü£¬Ė®ÖŠOŌŖĖŲ»ÆŗĻ¼ŪÓÉ-2¼Ū±äĪŖ0¼Ū£¬HŌŖĖŲ»ÆŗĻ¼ŪÓÉ+1¼Ū±äĪŖ0¼Ū£¬ĖłŅŌĖ®¼ČŹĒŃõ»Æ¼ĮÓÖŹĒ»¹Ō¼Į£»
¢Ū2F2+2H2O=O2+4HF£¬Ė®ÖŠOŌŖĖŲ»ÆŗĻ¼ŪÓÉ-2¼Ū±äĪŖ0¼Ū£¬ŌņĖ®×÷»¹Ō¼Į£»
¢Ü3NO2+H2O=2HNO3+NO ÖŠĖ®ÖŠø÷ŌŖĖŲ»ÆŗĻ¼Ū²»±ä£¬NŌŖĖŲ»ÆŗĻ¼ŪÓÉ+4¼Ū±äĪŖ+2¼Ū”¢+5¼Ū£¬ĖłŅŌĖ®¼Č²»ŹĒŃõ»Æ¼ĮÓÖ²»ŹĒ»¹Ō¼Į£»
¢ŻNaH+H2O=NaOH+H2”üÖŠĖ®ÖŠHŌŖĖŲ»ÆŗĻ¼ŪÓÉ+1¼Ū±äĪŖ0¼Ū£¬ŌņĖ®×÷Ńõ»Æ¼Į£»
¢Ž2Na2O2+2H2O=4NaOH+O2”üÖŠĖ®ÖŠø÷ŌŖĖŲ»ÆŗĻ¼Ū²»±ä£¬OŌŖĖŲ»ÆŗĻ¼ŪÓÉ-1¼Ū±äĪŖ-2¼Ū”¢0¼Ū£¬ĖłŅŌĖ®¼Č²»ŹĒŃõ»Æ¼ĮÓÖ²»ŹĒ»¹Ō¼Į£¬
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĮĖŃõ»Æ»¹Ō·“Ó¦£¬øł¾ŻŌŖĖŲ»ÆŗĻ¼Ū±ä»Æ½įŗĻ»ł±¾øÅÄī¼“æɽā“š£¬ÖŖµĄ³£¼ūŌŖĖŲ»ÆŗĻ¼Ū£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | °ŃÉ«²ŹĻŹŃŽµÄ×ÅÉ«¼ĮĢķ¼Óµ½Ó¤Ó׶łŹ³Ę·ÖŠ | |
| B£® | ×ö²ĖŹ±ÓĆŹŹĮæµÄŹ³ŃĪ”¢Ī¶¾«ŗĶ“×µ÷Ī¶ | |
| C£® | °Ń·¢Ć¹µÄ“óĆ×ɹøɲ¢ĢŌĻ“øɾ»ŗó×ö³ÉĢš¾ĘÉĻŹŠĻśŹŪ | |
| D£® | °Ń¹żĘŚŹ³Ę·ĻĀ¼Ü»ŲŹÕ£¬ÖŲŠĀÅēĀėŗóŌŁÉĻ¼ÜĻśŹŪ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 75.2% | B£® | 67.2% | C£® | 41.7% | D£® | 32.8% |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
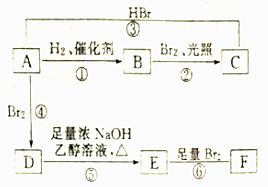
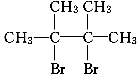
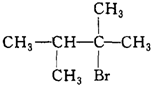 £®
£® £»Š“³öÓÉE”śFµÄ»Æѧ·½³ĢŹ½
£»Š“³öÓÉE”śFµÄ»Æѧ·½³ĢŹ½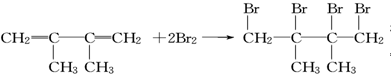 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K£ØHF£©=c£ØF-£©?c£ØH+£©/c£ØHF £© | B£® | K£ØHNO2£©=7.2”Į10-4 | ||
| C£® | ĖįŠŌĒæČõĪŖ HF£¾HNO2 | D£® | K£ØHNO2£©£¼K£ØHF£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
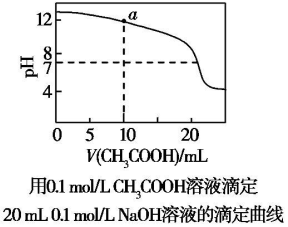
| A£® | pHĻąµČµÄCH3COONa”¢NaOHŗĶNa2CO3ČżÖÖČÜŅŗ£ŗc£ØCH3COONa£©£¼c£ØNa2CO3£©£¼c£ØNaOH£© | |
| B£® | H2AĪŖČõĖį£¬Ōņ0.1 mol£®L-1NaHAČÜŅŗÖŠ£ŗc£ØNa+£©=2c£ØA2-£©+c£ØHA-£©+c£ØH2A£© | |
| C£® | Ķ¼ÖŠpH=7Ź±£ŗc£ØNa+£©£¾c£ØCH3COO-£©£¾c£ØOH-£©=c£ØH+£© | |
| D£® | ÉĻĶ¼ÖŠaµćČÜŅŗ£ŗc£ØOH-£©=c£ØH+£©+c£ØCH3COO-£©+2c£ØCH3COOH£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ü¢Ż | B£® | Ö»ÓŠ¢Ł¢Ü | C£® | Ö»ÓŠ¢Ś¢Ū | D£® | Ö»ÓŠ¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚCH3COONa ČÜŅŗÖŠµĪČėĪŽÉ«·ÓĢŖ£¬ČÜŅŗ±äŗģ£ŗCH3COO-+H2O?CH3COOH+OH- | |
| B£® | ŌŚMg£ØOH£©2°×É«Šü×ĒŅŗÖŠµĪČė±„ŗĶFeCl3ČÜŅŗ£¬Šü×ĒŅŗ±äŗģŗÖ£ŗ3Mg£ØOH£©2+2Fe3+=2Fe£ØOH£©3+3Mg2+ | |
| C£® | ŌŚNaHSO3ČÜŅŗÖŠµĪ¼Ó×ĻÉ«ŹÆČļČÜŅŗ£¬ČÜŅŗ±äŗģ£ŗNaHSO3=Na++H++SO32- | |
| D£® | ŌŚ²ŻĖįČÜŅŗÖŠµĪČė¼øµĪĻ”H2SO4Ėį»ÆµÄKMnO4ČÜŅŗ£¬ČÜŅŗĪŽÉ«£ŗ2MnO4-+5H2C2O4+6H +=2Mn2++10CO2”ü+8H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
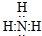 £¬ĀČ»Æļ§
£¬ĀČ»Æļ§ £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com