
| A、①②⑥ | B、④⑤ |
| C、③④⑦ | D、③④⑤⑦ |


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
| A、SO2、NOx、CO2、固体颗粒物同为大气污染物 |
| B、SO2对环境的主要影响是容易形成光化学烟雾,危害市民健康 |
| C、收集的酸雨在放置一段时间后pH会增大 |
| D、臭氧层是地球生命的保护伞,氟氯烃在破坏臭氧层时起到催化剂作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验次数 | 混合物的质量/g | 所加Ba(OH)2溶液的体积/L | 测得沉淀的质量/g |
| 1 | 0.858 | 0.5 | 1.379 |
| 2 | 1.716 | 0.5 | |
| 3 | 2.574 | 0.5 | 4.137 |
| 4 | 3.432 | 0.5 | 5.516 |
| 5 | 4.290 | 0.5 | 5.516 |
| 6 | 5.148 | 0.5 | 5.516 |
| 1 |
| 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 800℃ |
| 序号 | 1 | 2 | 3 | 4 | 5 | 6 |
| n(O2)的量 | a=4 | (3) | A≥5.5 | |||
| 残留固体 中含铜物质 | CuFeS2 Cu2S | (2) | Cu Cu2S | Cu | Cu Cu2O | |
| 物质的量 分别是多少 | (1) | (4) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 主 食 | 米 饭 |
| 副 食 | 红烧鱼 |
| 饮 品 | 豆 浆 |
| 你的补充 | ? |
查看答案和解析>>
科目:高中化学 来源: 题型:
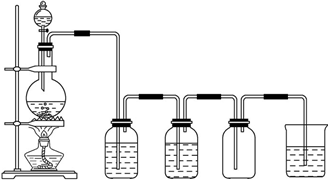
查看答案和解析>>
科目:高中化学 来源: 题型:
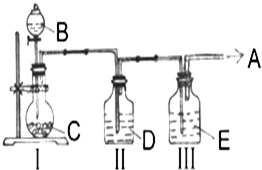 实验室中制取少量干燥纯净的气体A,可用如图装置
实验室中制取少量干燥纯净的气体A,可用如图装置查看答案和解析>>
科目:高中化学 来源: 题型:
| 成分 | 质量(g) | 摩尔质量(g?mol-1) |
| 蔗糖 | 68.4 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com