
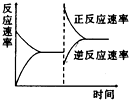
 如图是关于反应A2(g)+3B2(g)?2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是( )
如图是关于反应A2(g)+3B2(g)?2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是( )| A、升高温度,同时加压 |
| B、降低温度,同时减压 |
| C、增大反应物浓度,同时减小生成物浓度 |
| D、增大反应物浓度,同时使用催化剂 |


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
 25℃时,20mL0.1mol?L-1氨水溶液中逐滴加入0.2mol?L-1HCl溶液(如图),下列说法正确的是( )
25℃时,20mL0.1mol?L-1氨水溶液中逐滴加入0.2mol?L-1HCl溶液(如图),下列说法正确的是( )| A、在A、C间任一点,溶液中一定都有:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| B、在C点,c<10,且有c(NH4+)=c(Cl-)=c(OH-)=c(H+) |
| C、若25℃时 0.1mol/L 氨水电离度为1.33%,则b<a<12 |
| D、在D点:c(NH4+)+c(NH3?H2O)=2c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度℃ | 25 | 80 |
| 平衡常数 | 5×104 | 2 |
| A、上述反应的正反应为吸热反应 |
| B、25℃时反应Ni(CO)4(g)?Ni(s)+4CO(g)的平衡常数也为5×104 |
| C、在80℃时,测得某时刻,Ni(CO)4、CO浓度均为1mol.L-1,则此时v(正)>v(逆) |
| D、达平衡后,在容器中再加入一定的Ni粉,则平衡会向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(A)=5.0mol?L-1?min-1 |
| B、v(B)=2.0mol?L-1?min-1 |
| C、v(C)=0.9mol?L-1?s-1 |
| D、v(D)=1.0mol?L-1?s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、任何一个化学反应都能达到一个化学平衡状态 |
| B、当可逆反应在一定条件下达到最大限度是,正反应速率和逆反应速率相等 |
| C、平衡状态是一种静止的状态 |
| D、化学反应的限度不可能通过改变外界条件而改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 离子交换膜是一类具有离子交换功能的高分子材料,在生产和科研中有广泛应用.一容器被离子交换膜分成左右两部分,如图所示:
离子交换膜是一类具有离子交换功能的高分子材料,在生产和科研中有广泛应用.一容器被离子交换膜分成左右两部分,如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com