
【题目】新型钙钛矿太阳能电池是近几年来的研究热点,具备更加清洁、便于应用、制造成本低和效率高等显著优点,其中一种钙钛矿太阳能电池材料的晶胞如图。回答下列问题:
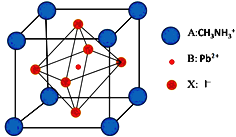
(1)铅或铅盐的焰色反应为绿色,下列有关原理分析的叙述正确的是_________(填字母)。
a.电子从基态跃迁到较高的激发态 b.电子从较高的激发态跃迁到基态
c.焰色反应的光谱属于吸收光谱 d.焰色反应的光谱属于发射光谱
(2)碳原子价层电子的轨道表达式(电子排布图)为_________。基态Pb原子核外电子排布,最后占据能级的电子云轮廓图形状为___________。
(3)CH3NH3+中含有化学键的类型有________(填字母序号),N原子的杂化形式为______,与CH3NH3+互为等电子体的分子为_________
a.极性键 b. 非极性键 c.配位键 d. 离子键 e.σ键 f.π键
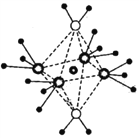
(4)NH4+中H—N—H的键角比NH3中H -N-H的键角大的原因是__________;NH3和水分子与铜离子形成的化合物中阳离子呈轴向狭长的八面体结构(如右图),该化合物加热时首先失去水,请从原子结构角度加以分析:__________。
(5)与I- 紧邻的I- 个数为__________。X射线衍射实验测得晶胞参数:密度为a g·cm-3,则晶胞的边长为____________pm(该物质的相对原子质量为M,NA表示阿伏加德罗常数的值)。
【答案】 bd  哑铃形 ace sp3杂化 C2H6或BH3NH3 NH4+中的氮原子上均为成键电子,而NH3分子中的氨原子上有一对孤对电子,孤对电子与成键电子之间的排斥力强于成键电子与成键电子之间的排斥力,导致NH4+中H-N-H的键角比NH3中大 由于O原子半径小,电负性大,提供孤对电子能力比N原子弱,故水分子形成的配位键弱于氨分子 8
哑铃形 ace sp3杂化 C2H6或BH3NH3 NH4+中的氮原子上均为成键电子,而NH3分子中的氨原子上有一对孤对电子,孤对电子与成键电子之间的排斥力强于成键电子与成键电子之间的排斥力,导致NH4+中H-N-H的键角比NH3中大 由于O原子半径小,电负性大,提供孤对电子能力比N原子弱,故水分子形成的配位键弱于氨分子 8 ![]()
【解析】(1)铅或铅盐的焰色反应为绿色,是因为金属及其盐在火焰上灼烧时,原子中的电子吸收了能量,从能量较低的轨道跃迁到能量较高的轨道,但处于能量较高的轨道上的电子是不稳定的,很快跃迁回能量较低的轨道,这时就将多余的能量以光的形式释放出来,呈现特殊的颜色,其光谱属于发射光谱,故选bd。
(2)根据核外电子排布规律可知碳原子价层电子的轨道表达式(电子排布图)为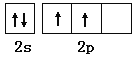 。基态Pb原子核外电子排布,最后占据能级的电子为6p能级,因此电子云轮廓图形状为哑铃形。
。基态Pb原子核外电子排布,最后占据能级的电子为6p能级,因此电子云轮廓图形状为哑铃形。
(3)同种非金属元素之间存在非极性键,不同非金属元素之间存在极性键,含有孤电子对和含有空轨道的原子之间存在配位键,共价单键为σ键,共价双键含有一个σ键和一个π键,所以CH3NH3+中碳氮原子之间,碳氢原子之间及氮氢原子之间存在极性键和σ键,氮氢之间含有配位键,故选ace,N连接4个单键,杂化形式为sp3,CH3NH3+为18电子微粒,与CH3NH3+互为等电子体的分子为C2H6或BH3NH3。
(4)NH4+中的氮原子上均为成键电子,而NH3分子中的氨原子上有一对孤对电子,孤对电子与成键电子之间的排斥力强于成键电子与成键电子之间的排斥力,导致NH4+中H-N-H的键角比NH3中大。由于O原子半径小,电负性大,提供孤对电子能力比N原子弱,故水分子形成的配位键弱于氨分子。
(5)由晶胞结构可知,I-位于晶胞的面心,由于8个晶胞共用一个顶点,所以与I- 紧邻的I- 个数为8个;设晶胞的边长为x pm,则晶胞的体积为x3![]() 10-30 cm-3,晶胞中含有一个CH3NH3+(8
10-30 cm-3,晶胞中含有一个CH3NH3+(8![]() =1)、一个Pb2+(体心)、三个I-(6
=1)、一个Pb2+(体心)、三个I-(6![]() =3)所以有a g·cm-3
=3)所以有a g·cm-3![]() x3
x3![]() 10-30 cm3NA=M
10-30 cm3NA=M
解得x=![]() ,因此,本题答案为:8 ;
,因此,本题答案为:8 ; ![]() 。
。


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】H2C2O4(乙二酸),俗名草酸,存在于自然界的植物中。已知常温下草酸电离平衡常数K1=5.0×10-2,K2=5.4×10-5,碳酸的电离平衡常数K1=4.5×10-7,K2=4.7×10-11。Ksp (CaC2O4)=2.3×10-9,Ksp(CaCO3)=2.5×10-9。回答下列问题:
(1)写出草酸溶液中存在的主要电离反应方程式_____________________________________。
(2)长期将豆腐与菠菜混合食用,容易损失钙素且患胆结石疾病。理由是______________________。
(3)25℃,物质的量浓度均为0.1mol/L 的Na2C2O4溶液的pH比Na2CO3溶液pH_________(填“大”“ 小”或“相等”)。将上述两种溶液等体积混合后,滴加CaCl2溶液,当C2O42- 沉淀完全时,CO32-是否沉淀完全_______________(填“是”或“否”)
(4)写出NaHC2O4溶液中水解反应的离子方程式________________________________,计算常温下该反应的水解平衡常数为_____________________,NaHC2O4溶液的pH____7 (填“>”、“<”或“=”)
(5)向盛有饱和草酸溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液的紫红色褪去,写出该反应的离子方程式________________________________________。
(6)设计实验证明草酸的酸性比碳酸强________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是283.0 kJ/mol,则2CO(g)+O2(g) =2CO2(g)反应的ΔH=—(2×283.0)kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于区域3的是

A. 4FeS2+11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
B. 2Na+Cl2![]() 2NaCl
2NaCl
C. Zn+CuSO4===ZnSO4+Cu
D. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A的质谱图中,质荷比最大的数值为42。碳氢两元素的质量比为6:1,其核磁共振氢谱有三个峰,峰的面积比为1:2:3。A与其他有机物之间的关系如下:

已知:CH2=CH2![]() HOCH2CH2OH,回答下列问题:
HOCH2CH2OH,回答下列问题:
(1)有机物B的分子式___________________________。
(2)高聚物F结构简式为___________________。
(3)写出C与新制的氢氧化铜反应的化学方程式___________________________。
(4)E在一定条件下可以相互反应生成一种六元环有机物H,H的结构简式________.。
(5)写出生成G的化学方程式_____________________________________________;
【答案】 )C3H8O2 ![]()
![]()
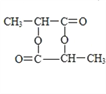 n
n![]()
![]()
![]() +(n-1)H2O
+(n-1)H2O
【解析】试题分析:本题考查有机推断,涉及有机物分子式和结构简式的确定、有机物分子式和结构简式的书写、有机反应方程式的书写。A的质谱图中质荷比最大的数值为42,A的相对分子质量为42,烃A中n(C):n(H)=![]() :
: ![]() =1:2,A的实验式为CH2,A的分子式为(CH2)x,14x=42,解得x=3,A的分子式为C3H6,A的核磁共振氢谱有三个峰且峰的面积比为1:2:3,A的结构简式为CH2=CHCH3。A发生加聚反应生成的高聚物F的结构简式为
=1:2,A的实验式为CH2,A的分子式为(CH2)x,14x=42,解得x=3,A的分子式为C3H6,A的核磁共振氢谱有三个峰且峰的面积比为1:2:3,A的结构简式为CH2=CHCH3。A发生加聚反应生成的高聚物F的结构简式为![]() ;A→B发生题给已知的反应,B的结构简式为
;A→B发生题给已知的反应,B的结构简式为![]() ;B→C发生醇的催化氧化,C的结构简式为
;B→C发生醇的催化氧化,C的结构简式为![]() ;C与Cu(OH)2加热时,C中-CHO被氧化,酸化后得到的D的结构简式为
;C与Cu(OH)2加热时,C中-CHO被氧化,酸化后得到的D的结构简式为![]() ;D与H2发生加成反应生成E,E的结构简式为
;D与H2发生加成反应生成E,E的结构简式为![]() ;E中含羟基和羧基,E发生缩聚反应生成高聚物G,G的结构简式为
;E中含羟基和羧基,E发生缩聚反应生成高聚物G,G的结构简式为![]() 。
。
(1)B的结构简式为![]() ,B的分子式为C3H8O2。
,B的分子式为C3H8O2。
(2)高聚物F的结构简式为![]() 。
。
(3)C的结构简式为![]() ,C与新制Cu(OH)2反应的化学方程式为
,C与新制Cu(OH)2反应的化学方程式为![]() +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH![]()
![]() +Cu2O↓+3H2O。
+Cu2O↓+3H2O。
(4)E的结构简式为![]() ,2分子E通过酯化反应形成六元环有机物H,H的结构简式为
,2分子E通过酯化反应形成六元环有机物H,H的结构简式为 。
。
(5)G由E发生缩聚反应生成,生成G的化学方程式为n![]()
![]()
![]() +(n-1)H2O。
+(n-1)H2O。
【题型】推断题
【结束】
18
【题目】苯甲酸乙酯(C9H10O2)稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为:
已知: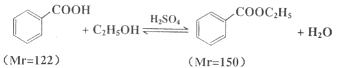
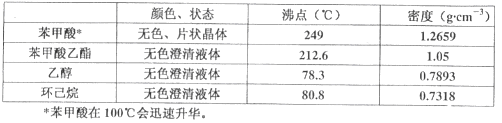

实验步骤如下:①在100 mL圆底烧瓶中加入12.20 g苯甲酸、25mL乙醇(过量)、20mL环己烷,以及4mL浓硫酸,混合均匀并加入沸石,按左上图所示装好仪器,控制温度在65~70℃加热回流2h。反应时环己烷-乙醇-水会形成“共沸物”(沸点62.6℃)蒸馏出来。再利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞。继续加热,至分水器中收集到的液体不再明显增加,停止加热。
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性。
④用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并有机层。加入氯化钙,对粗产品进行蒸馏(装置如图所示)。低温蒸出乙醚后继续升温,接收210~213℃的馏分。
⑤检验合格,测得产品体积为12.86mL.
(1)步骤①中使用分水器不断分离除去水的目的是_________________。
(2)步骤②中应控制馏分的温度在___________________。
A.65~70℃ B.78~80℃ C.85~90℃ D.215~220℃
(3)步骤③中若Na2CO3加入不足,在步骤④蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是_____________。
(4)步骤④中分液操作叙述正确的是__________。
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞。将分液漏斗倒转用力振摇
B.振摇几次后需打开分液漏斗下口的玻璃塞放气
C.经几次振摇并放气后,手持分液漏斗静置待液体分层
D.分液操作时,分液漏斗中的下层液体由下口放出,然后再将上层液体由下口放出
蒸馏装置图中仪器A的名称是___________,在步骤④中加入氯化钙的作用是_________。
(5)该实验产品的产率为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
(1)还原剂是________,还原产物__________。
(2)浓硝酸在反应中表现出来的性质是________________。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(3)当有9.6g铜参与反应时,在标准状况下,产生气体的体积为________,转移的电子数为___________。
(4)用双线桥法标出电子转移的方向和数目______。
Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用电化学法制备LiOH的实验装置如图,采用惰性电极,a口导入LiCl溶液,b口导入LiOH溶液,下列叙述正确的是( )

A.通电后阳极区溶液pH增大
B.阴极区的电极反应式为4OH-–4e-=O2↑+2H2O
C.当电路中通过1mol电子的电量时,会有0.25mol的Cl2生成
D.通电后Li+通过交换膜向阴极区迁移,LiOH浓溶液从d口导出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学常见的滴定法包括中和滴定法、氧化还原反应滴定法等。
(1)探究小组甲用酸性KMnO4溶液滴定某补血剂[主要成分硫酸亚铁晶体(FeSO47H2O)]中铁元素的含量。
①下列滴定装置中(夹持部分略去),最合理的是:__________(填字母序号)。
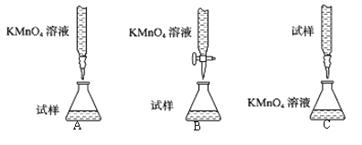
②该小组拟在同浓度的FeSO4溶液中,探究酸性KMnO4溶液浓度对Fe2+被氧化时反应速率的影响。限选试剂与仪器:0.10molL-1FeSO4、0.02molL-1酸性KMnO4、蒸馏水、锥形瓶、试管、胶头滴管、量筒、秒表。参照下表格式,完成实验表格(列出所选试剂体积和数据;数据用字母表示)。_____________、_____________、_____________、_____________。

(2)常温下,探究小组乙将0.1 mol·L-1盐酸滴入20 mL 0.1 mol·L-1氨水中,溶液的pH随加入盐酸体积的变化曲线如图所示。
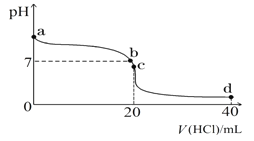
①a点处假设溶液的pH=10,则该点处由水电离产生的c(OH-)=__________________。
②取c点时的饱和溶液并向其加入水玻璃(硅酸钠水溶液),振荡、静置。写出实验现象并用必要的文字和相关离子方程式给予解释:___________________________________。
③d点所示溶液中离子浓度由大到小的排序是_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com