
| A. | 中子数为20的氯原子:${\;}_{17}^{37}$Cl | |
| B. | 碳酸钠水解的离子方程式:CO32-+2H2O?OH-+H2CO3 | |
| C. | CH3COOH的电离方程式为:CH3COOH+H2O?CH3COO-+H3O+ | |
| D. | 次氯酸的结构式:H-O-Cl |
分析 A.元素符号的左上角标质量数,质量数=质子数+中子数;
B.碳酸钠为盐,完全电离,碳酸根离子水解分步进行,以第一步为主,不能一步完成;
C.CH3COOH是弱酸部分电离,H3O+为水合氢离子;
D.HClO中Cl原子只形成1个共价键.
解答 解:A.氯元素的质子数为17,中子数为20的氯原子的质量数=17+20=37,该原子正确的表示方法为:1737Cl,故A正确;
B.碳酸钠为盐,完全电离,碳酸根离子水解分步进行,以第一步为主:CO32-+H2O?HCO3-+OH-,第二步水解为:HCO3-+H2O?H2CO3+OH-,故B错误;
C.CH3COOH是弱酸在溶液中部分电离,其电离方程式为:CH3COOH?CH3COO-+H+,H3O+为水合氢离子,或写成CH3COOH+H2O?CH3COO-+H3O+,故C正确;
D.次氯酸分子中存在1个氢氧键和1个氧氯键,其结构式为:H-O-Cl,故D正确;
故选B.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及原子符号、水解离子方程式、电离方程式、结构式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | SO2和NO2是主要的大气污染物 | |
| B. | 大气中的SO2和CO2溶于水形成酸雨 | |
| C. | 以液化石油气代替燃油可减少大气污染 | |
| D. | 对煤燃烧后形成的烟气脱硫,目前主要用石灰法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
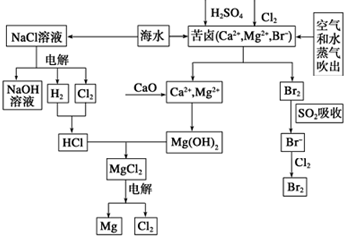 海水是宝贵的资源宝库,目前氯碱工业、海水提镁、海水提溴为人类提供了大量工业原料.下图是海水综合利用的部分流程图,据图回答问题:
海水是宝贵的资源宝库,目前氯碱工业、海水提镁、海水提溴为人类提供了大量工业原料.下图是海水综合利用的部分流程图,据图回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | CH3COOH | H2CO3 | H2SO3 |
| 电离平衡常数K | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②④ | C. | ②③④ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C4H10(g)+O2(g)═4CO2(g)+5H2O(l)△H=-QkJ•mol-1 | |
| B. | C4H10(g)+O2(g)═4CO2(g)+5H2O(l)△H=-10QkJ•mol-1 | |
| C. | C4H10(g)+O2(g)═4CO2(g)+5H2O(l)△H=+10QkJ•mol-1 | |
| D. | C4H10(g)+O2(g)═4CO2(g)+5H2O(g)△H=-10QkJ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2 | 20 | |
| Ⅱ | 2 | 20 | 10滴饱和MnSO4溶液 |
| Ⅲ | 2 | 30 | |
| Ⅳ | 1 | 20 | 1mL蒸馏水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com