
| A、NaHCO3 |
| B、FeCl3 |
| C、Mg (NO3)2 |
| D、Al2(SO4)3 |


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
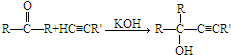 已知:
已知: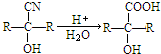
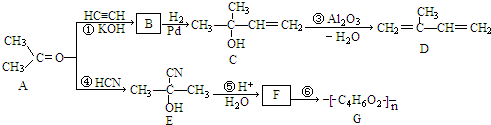
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 规律 | 结论 |
| A | 较强酸可以制取较弱酸 | HClO不能制取HCl |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C | 还原剂的还原性一定大于还原产物 | 工业上通常用钠与熔融氯化钾反应制取钾 |
| D | 溶解度小的沉淀易向溶解度更小的沉淀转化 | 自然界闪锌矿PbS遇到CuSO4溶液可以转变为铜蓝CuS |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
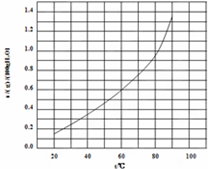
| A、溴酸银的溶解是放热过程 |
| B、温度升高时溴酸银溶解速度加快 |
| C、60℃时溴酸银的KSP约等于6.25×10-4 |
| D、若硝酸钾中含有少量溴酸银,可用重结晶方法提纯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、因为氯气有毒,所以氯气可用于自来水的杀菌消毒 |
| B、氯气可使湿润的红布条退色,但氯气本身不具有漂白性 |
| C、在通常情况下,氯气可以和任何金属直接化合 |
| D、闻其气味时要小心将集气瓶放在鼻孔下直接闻 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在化学反应中,只有能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察图1然后回答问题.
在化学反应中,只有能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察图1然后回答问题.| 化学键 | H-S | S-S | S=O | H-O |
| 键能/KJ?mol-1 | 364 | 266 | 522 | 464 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3 溶液中投入过量Na:Al3++4Na+2H2O═AlO2-+4Na++2H2↑ |
| B、苯酚钠溶液中通入少量CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- |
| C、硫化钠的水解反应:S2-+H2O?HS-+OH- |
| D、NaClO 溶液中通入过量SO2:ClO-+SO2+H2O═HClO+HS03- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com