
【题目】锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231℃;Sn2+易水解、易被氧化。请按要求回答下列相关问题:
(1)SnSO4可使酸性KMnO4溶液褪色,该过程中Sn2+转化为Sn4+,该反应的离子方程式为_______。
(2)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:

①步骤Ⅰ加入Sn粉的作用: _______________________。
②步骤Ⅱ用到的玻璃仪器有烧杯、_____________________________。
③步骤Ⅲ生成SnO的离子方程式:_________________________。
④步骤Ⅳ中检验SnO是否洗涤干净的操作是____________________,证明已洗净。
⑤步骤Ⅴ由SnSO4溶液得到SnSO4晶体的操作依次为 ________ 、 ________、过滤、洗涤、低温干燥。
【答案】 5Sn2++2MnO4-+16H+=5Sn4++2Mn2++8H2O 防止Sn2+被氧化为Sn4+ 漏斗、玻璃棒 Sn2++2HCO3-==SnO↓+2CO2↑+H2O 取最后一次洗涤液少许于试管中,加入足量的HNO3酸化的AgNO3溶液,若无白色沉淀,则已洗净,反之则没有洗净 蒸发浓缩 冷却结晶
【解析】(1)、SnSO4可使酸性KMnO4溶液褪色,该过程中Sn2+转化为Sn4+,说明KMnO4作氧化剂,生成Mn2+,故其反应的离子方程式是:5Sn2++2MnO4-+16H+=5Sn4++2Mn2++8H2O。
(2)、①.由于Sn2+易水解、易被氧化,加入盐酸,抑制Sn2+水解,加入Sn粉可以与盐酸反应,调节溶液pH,还可以防止Sn2+被氧化为Sn4+,故答案是:防止Sn2+被氧化为Sn4+。
②.步骤Ⅱ为过滤,过滤需要用到的玻璃仪器是烧杯、漏斗、玻璃棒,故答案是:漏斗、玻璃棒。
③. 得到沉淀是SnO,Sn元素化合价未发生变化,属于非氧化还原反应,变质发生水解反应生成Sn(OH)2与二氧化碳,Sn(OH)2再脱水得到SnO,反应离子方程为:Sn2++2HCO3=SnO↓+2CO2↑+H2O,故答案为:Sn2++2HCO3=SnO↓+2CO2↑+H2O;
④. 沉淀为SnO,表面附着有Cl,要想检验滤渣是否洗涤干净,可以用硝酸、硝酸银溶液检验最后一次洗涤液中是否含有Cl,具体方案为:取最后一次滤液少许于试管中,依次滴加足量硝酸酸化的硝酸银溶液,观察到无白色沉淀,说明洗涤干净,反之则没有洗净。
故答案为:取最后一次洗涤液少许于试管中,加入足量的HNO3酸化的AgNO3溶液,若无白色沉淀,则已洗净,反之则没有洗净。
⑤.由流程图可知,操作V是由SnSO4溶液得到SnSO4晶体,只能采取蒸发浓缩、冷却结晶、过滤、洗涤得到,故答案为:蒸发浓缩、冷却结晶。


科目:高中化学 来源: 题型:
【题目】将0.1 mol的镁、铝混合物溶于100 mL 2mol/L H2SO4溶液中,然后再滴加1 mol/L NaOH溶液。请回答:
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如下图所示。

当V1=160mL时,则金属粉末中n(Mg)=________ mol,V2=_____________mL。
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH) _____________mL。
(3)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某物质E可做香料,其结构简式为![]() ,工业合成路线如下:
,工业合成路线如下:
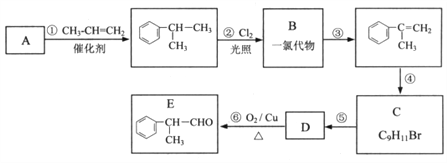
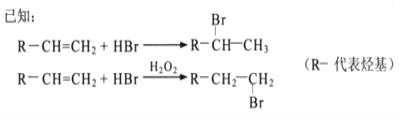
回答下列问题:
(1)A为芳香烃,相对分子质量为78。下列关于A的说法中,正确的是__________(填序号);
a. 所有原子均在同一平面上 b. 密度比水大 c. 一氯代物只有一种
(2)B的结构简式可能是____________________ 、_________________;
(3)D的结构简式为:________________________;
(4)步骤④的化学方程式是____________________________________________;
(5)步骤⑥的化学方程式是____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用焰色反应,人们在烟花中有意识地加入特定金属元素,使焰火更加绚丽多彩。下列说法中正确的是
A. 非金属单质燃烧时火焰均为无色
B. 焰色反应每次实验都要用稀盐酸洗净铂丝
C. 焰色反应均应透过蓝色钴玻璃观察
D. 只有金属单质灼烧时火焰才有颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将CO2气体缓缓地通入到含KOH、Ba(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示。下列关于整个反应进程中的各种描述不正确的是( )

A. o—a段反应的化学方程式是:Ba(OH)2+ CO2===BaCO3↓+ H2O
B. b—c段反应的离子方程式是:2AlO2-+ 3H2O+ CO2===2Al(OH)3↓+ CO32-
C. a—b段与c—d段所发生的反应相同
D. d—e段沉淀的减少是由于碳酸钡固体的消失所致
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质A~I之间能发生如下反应(图中部分反应的条件和产物没有全部标出),其中A,B,C,I为金属单质,B是地壳中含量最多的金属,甲、乙、丙为气体. 
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:C、H .
(2)写出气体甲在气体乙中燃烧的化学方程式:;该反应的现象有: .
(3)写出反应③的化学方程式:;向反应③所得溶液中通入过量的CO2 , 写出反应的离子方程式: .
(4)写出反应⑤的离子方程式:;
(5)检验物质D中阳离子的方法名称是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Na+浓度为0.5molL﹣1的某澄清溶液中,还可能含有下表中的若干种离子:
阳离子 | K+、Ag+、Mg2+ |
阴离子 | NO3﹣、CO32﹣、SiO32﹣、SO42﹣ |
取该溶液100mL进行如下实验(气体体积在标准状况下测定):
序号 | 实验内容 | 实验结果 |
Ⅰ | 向该溶液中加入足量稀HCl | 产生白色沉淀并放出0.56L气体 |
Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
Ⅲ | 在Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
试回答下列问题:
(1)实验Ⅰ能确定一定不存在的离子是 .
(2)实验Ⅰ中生成沉淀的离子方程式为 .
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)
阴离子 | NO3﹣ | CO32﹣ | SiO32﹣ | SO42﹣ |
c/molL﹣1 |
(4)判断原溶液中K+是否存在,若存在,求其最小物质的量浓度,若不存在,请说明理由: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0试回答下列问题:
CO2(g)+H2(g) ΔH<0试回答下列问题:
(1)若起始时c(CO)=2 mol/L,c(H2O)=3 mol/L,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K=____________。
(2)在相同温度下,若起始时c(CO)=1 mol/L,c(H2O)=2 mol/L,反应进行一段时间后,测得H2的浓度为0.5 mol/L,则此时该反应是否达到平衡状态________(填“是”或“否”),此时v(正)________v(逆)(填“大于”“小于”或“等于”)。
(3)若降低温度,该反应的K值将________,该反应的化学反应速率将________(均填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A. 0.1mol/L的NaClO溶液中含有C1O-的数目小于NA
B. 标准状况下,将22.4LC12通入水中,发生反应后,转移的电子数为NA
C. 100g46%的乙醇溶液中,含H-O键的数目为NA
D. 4.6gNa在空气中完全反应生成Na2O、Na2O2,转移0.2NA个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com