
| 物质 | 乙醇 | 四氯化碳 | 裂化汽油 | 碘(晶体) |
| 密度/g•cm-3 | 0.789 | 1.595 | 0.71~0.76 | 4.93 |
| 沸点/℃ | 78.5 | 76.8 | 25~232 | 184.35 |
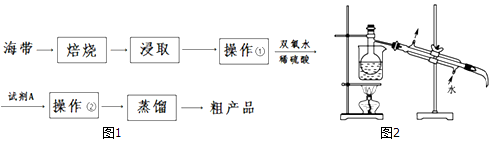
分析 (1)灼烧海带需要的仪器有:酒精灯、三脚架、泥三角及坩埚;
(2)浸取液中主要含有碘离子,与足量的双氧水和稀硫酸作用,会发生氧化还原反应,反应中I元素的化合价升高,O元素的化合价降低;
(3)分离不溶性固体和液体的方法是过滤,所以操作①为过滤,过滤需要用到的玻璃仪器有漏斗、玻璃棒和烧杯;
(4)操作②为萃取分液,萃取剂的选取标准是:溶质在萃取剂中的溶解度大于在原溶剂中的溶解度,溶质和萃取剂不反应,萃取剂和原来溶剂不能互溶;
(5)根据蒸馏操作方法判断需要仪器名称,然后找出还缺少的玻璃仪器名称;
(6)2KClO3+I2=2KIO3+Cl2中,Cl元素的化合价由+5价降低为0,I元素的化合价由0升高为+5,结合氧化还原反应中的基本概念来解答.
解答 解:实验室从海带提取碘:海带焙烧成灰,浸泡溶解得到海带灰悬浊液,含有碘离子,加入酸和氧化剂,足量的稀硫酸和双氧水将碘离子氧化成碘单质,通过操作①过滤,得到不溶的残渣,滤液为碘单质溶液,利用有机溶剂A四氯化碳萃取出碘单质,再通过蒸馏提取出碘单质.
(1)灼烧海带用坩埚盛放海带,用带铁圈的铁架台放置泥三角,泥三角上放置坩埚,用酒精灯进行加热,所以焙烧海带时需要用到的实验仪器是坩埚、带铁圈的铁架台、酒精灯、泥三角,无需用到的仪器有烧杯、蒸发皿,
故答案为:CE;
(2)焙烧所得的紫菜灰主要含有碘离子,与足量的双氧水和稀硫酸作用,会发生氧化还原反应,方程式为:2I-+H2O2+2H+=I2+2H2O,
故答案为:2I-+H2O2+2H+═I2+2H2O;
(3)操作①为过滤,过滤所用的玻璃仪器是烧杯、漏斗和玻璃棒,所以除用到玻璃棒外,还需要的玻璃仪器有烧杯、漏斗,
故答案为:烧杯、漏斗;
(4)操作②主要是把碘单质从水中萃取到四氯化碳溶液中,然后再分液,题干中提供的四中物质,乙醇和水能互溶,不能做萃取剂,裂化汽油含有不饱和碳碳双键能与碘发生加成反应,不能做萃取剂,四氯化碳符合萃取剂的选取标准,所以可以用四氯化碳作萃取剂,
故答案为:四氯化碳;
(5)蒸馏操作中用到的仪器有:酒精灯、蒸馏烧瓶、温度计、冷凝管、尾接管、锥形瓶,还缺少的玻璃仪器为:温度计、锥形瓶,
故答案为:温度计、锥形瓶;
(6)2KClO3+I2=2KIO3+Cl2中,Cl元素的化合价由+5价降低为0,I元素的化合价由0升高为+5,
A.元素的非金属性越强,则单质的氧化性越强,非金属性:Cl>I,则氧化性:Cl2>I2,故A错误;
B.由反应可知,每生成1 mol KIO3转移的电子数为(5-0)=5mole-,故B正确;
C.一种单质与一种化合物反应生成另一种单质和另一种化合物的反应为置换反应,则该反应是置换反应,故C正确;
D.KClO3和KIO3中含有离子键和共价键,故D正确;
故答案为:A.
点评 本题考查了从海带中提取碘实验方案设计,涉及物质的分离、检验、仪器的选取等知识点,根据物质的特点及性质选取相应的分离和检验方法,根据仪器的作用选取仪器,注意把握实验流程和实验原理,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | CH3CH2Br→CH3CH2OH→CH2=CH2$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| B. | CH3CH2Br$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| C. | CH3CH2Br→CH2=CH2 $\stackrel{HBr}{→}$CH2BrCH3$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| D. | CH3CH2Br→CH2=CH2 $\stackrel{Br_{2}}{→}$CH2BrCH2Br |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验时可观察到试纸变蓝 | |
| B. | 实验可证明该条件下I-可被IO3-氧化 | |
| C. | 上述反应中氧化剂和还原剂的物质的量之比为1:5 | |
| D. | 可根据元素周期律推断出酸性:HIO3<HClO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氮的重要化合物,如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等在生产、生活中具有重要作用.
氮的重要化合物,如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等在生产、生活中具有重要作用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙溶于醋酸溶液:CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 镁溶于浓NH4Cl溶液:2NH4++Mg=2NH3↑+H2↑+Mg2+ | |
| C. | 用两个铜电极电解Cu(NO3)2溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu↓+4H++O2↑ | |
| D. | 向25mL沸水中滴入5~6滴饱和FeCl3溶液,再煮沸至液体呈透明红褐色:Fe3++3H2O?Fe(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取10.00 mL硫酸:在25mL酸式滴定管中装入硫酸,调整初始读数为15.00mL后,将剩余硫酸放入锥形瓶 | |
| B. | 用乙酸浸泡水壶中的水垢,可将其清除,可以得出结论乙酸的酸性大于碳酸的酸性 | |
| C. | SO2的水溶液能够导电,所以SO2是电解质 | |
| D. | 测定醋酸溶液pH用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com