
在标准状况下,向体积为V L的容器中放入a mol CS2液体和b mol O2,待燃烧后恢复到开始时的温度和压强条件时,容器中气体的物质的量为 ( )
A.a mol B. b mol
C.(3a-b) mol D.(a+b) mol
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
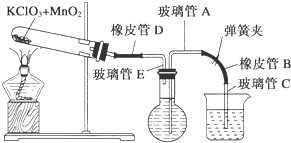 测定1mol氧气在标准状况下所占体积的实验操作的步骤如下:①按如图装配实验装置.②洗净试管然后充分干燥.
测定1mol氧气在标准状况下所占体积的实验操作的步骤如下:①按如图装配实验装置.②洗净试管然后充分干燥.查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:013
(A)a摩 (B) b摩
(C)(3a-b)摩 (D)(a+b)摩
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:013
A.a mol B. b mol
C.(3a-b) mol D.(a+b) mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com