
【题目】肼(N2H4)在不同条件下分解产物不同,200℃时在Cu表面分解的机理如图1。已知200℃时:
反应 I : 3N2H4(g)=N2(g)+4NH3(g) △Hl=-32.9kJ/mol
反应II: N2H4(g)+H2(g)=2NH3(g) △H2=-41.8 kJ/mol

下列说法不正确的是
A. 图l所示过程①、②都是放热反应
B. 反应Ⅱ的能量过程示意图如图2所示
C. 断开3 molN2H4(g)中的化学键吸收的能量大于形成1 molN2(g)和4 molNH3(g)中的化学键释放的能量
D. 200℃时,肼分解生成氨气和氢气的热化学方程式为N2H4(g) =N2(g)+2H2 (g) △H=+50.7 kJ/mol
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】几种物质的溶度积常数见下表:

(1)某酸性CuCl2溶液中含少量的FeCl3,为制得纯净CuCl2溶液,宜加入_______调至溶液pH=4,使Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=____________________________。
(2)过滤后,将所得滤液经过________________操作,可得到CuCl2·2H2O晶体。
(3)由CuCl2·2H2O晶体得到纯的无水CuCl2,需要进行的操作是________________。
(4)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.800 g试样溶于水,加入过呈KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液40.00 mL。(已知:I2+2S2O![]() ===S4O
===S4O![]() +2I-)。
+2I-)。
①可选用________作滴定指示剂,滴定终点的现象是__________________________。
②CuCl2溶液与KI反应的离子方程式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是实验室制备气体的有关内容:
编号 | 实验内容 | 实验原理 | 气体发生装置 |
① | 制氧气 | H2O2―→O2 | |
② | 制氨气 | NH4Cl―→NH3 | |
③ | 制氯气 | HCl―→Cl2 |
(1)上表气体中:从制备过程看,必须选择合适的氧化剂才能实现的是____填气体的化学式,下同);从反应原理看,明显不同于其他两种气体的是________。
(2)根据表中所列实验原理,从下列装置中选择合适的气体发生装置,将其编号填入上表中的空格中_______。
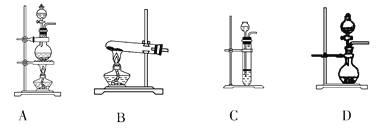
(3)若用上述制备O2的装置制备NH3,则选择的试剂为________________。
(4)制备Cl2需用8 mol·L-1的盐酸100 mL,现用12 mol·L-1的盐酸来配制。
①为提高配制的精确度,量取浓盐酸的仪器可选用下列中的______填序号):

②配制过程中,除上图所列仪器外,还需要的仪器有________、________、______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:
MnO2+4HCI(浓)![]() MnCl2+C12↑+2H2O
MnCl2+C12↑+2H2O
取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为6.72L。
请回答下列问题:
(1)参加反应的二氧化锰的质量为 。
(2)参加反应的HCl的物质的量为 。
(3)实验室备用的浓盐酸质量分数为36.5%,密度为1.19g·cm-3, 为使用方便,请计算出该浓盐酸的物质的量浓度: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:
Pb+PbO2+4H++2SO42-![]() 2PbSO4+2H2O,
2PbSO4+2H2O,

则下列说法正确的是:
A. 放电时:电子流动方向由A经导线流向B
B. 放电时:正极反应是Pb-2e-+SO42-PbSO4
C. 充电时:铅蓄电池的负极应与充电器电源的正极相连
D. 充电时:阳极反应是PbSO4-2e-+2H2OPbO2+SO42-+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中错误的是( )
A.阿伏加德罗常数的数值与12g 12C所含的碳原子数相等
B.在0.5mol Na2SO4 中,含有的Na+ 数约是6.02×1023
C.等物质的量的O2 与O3 , 所含氧原子数相等
D.摩尔是物质的量的单位
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作会促进H2O的电离,且使溶液pH>7的是:
A. 将纯水加热到90 ℃ B. 向水中加少量Na2CO3固体
C. 向水中加少量NaOH固体 D. 向水中加少量FeCl3固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】发射卫星的火箭推进器中大多使用燃料偏二甲肼,其化学式C2H8N2。
计算:(1)偏二甲肼的摩尔质量是________;480 g偏二甲肼的物质的量为 ________。
(2)偏二甲肼中碳原子与氮原子的个数之比是________,其物质的量之比是 ________;1mol偏二甲肼中含有的氢原子数目是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com