
| A、合成氨反应需使用催化剂,说明催化剂可以促进该平衡向生成氨的方向移动 |
| B、常温下,将pH=10的氨水稀释,溶液中所有离子浓度都减小 |
| C、100 mL pH=3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明HA酸性比HB弱 |
| D、Fe2+与[Fe(CN)6]3-反应生成红色的铁氰化亚铁沉淀 |


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
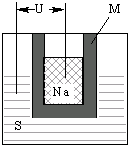
| A、Na电极为电池负极,S电极为电池正极 | ||
B、电池放电时,正极反应为xS+2e-═S
| ||
| C、电池充电时.Na所在电极连接电源正极 | ||
| D、M的作用为导电和隔离钠和硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C5H12有2种同分异构体 |
| B、C8H10中只有三种属于芳香烃的同分异构体 |
| C、甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种 |
| D、CH3CH2CH2CH3光照下与氯气反应,只生成一种一氯代烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH由小到大的顺序是①<②<③<④ |
| B、溶液中水电离出的H+浓度由小到大的顺序是②<①<④<③ |
| C、取一定体积的④溶液,分别和①、②、③溶液完全中和,消耗①、②、③溶液的体积由小到大的顺序是②<①<③ |
| D、取a体积的①溶液和b体积的④溶液混合后,溶液的pH为3,则a:b约为11:9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na,Mg,Al金属性依次减弱 |
| B、HCl,H2S,PH3稳定性依次减弱 |
| C、NaOH,KOH,CsOH碱性依次减弱 |
| D、S2-,Cl-,Ca2+半径依次减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
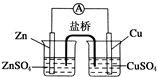
| A、锌电极发生还原反应,铜电极发生氧化反应 |
| B、盐桥中的阴离子向硫酸铜溶液中迁移 |
| C、电子从锌电极通过电流计流向铜电极 |
| D、铜电极上发生的电极反应为2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性强弱:HClO4>H2SO4>H3PO4 |
| B、离子半径:Na+>Mg2+>Al3+>F- |
| C、热稳定性:HCl>H2S>PH3>SiH4 |
| D、碱性强弱:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com