

| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 | HVO3 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 | 难溶 |
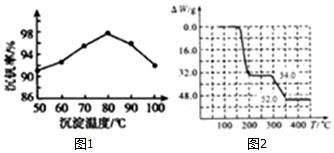
分析 废钒催化剂粉碎、水浸,将溶解性物质溶于水,然后过滤得到滤渣和滤液,根据溶解性表知,滤液中含有VOSO4,滤渣中含有V2O5等不溶性杂质,向滤渣中加入亚硫酸钠和稀硫酸,亚硫酸钠具有还原性,能将V2O5还原为VOSO4,然后过滤得到滤渣和滤液,将两部分滤液混合并加入氯酸钾,氯酸钾具有氧化性,能将VOSO4氧化为(VO2)2SO4,调节溶液pH为8且采用离子交换方法得到VO3-,向溶液中加入氯化铵,得到难溶性的NH4VO3,焙烧NH4VO3得到V2O5,
(1)工业由V2O5冶炼金属钒常用铝热剂法,铝和五氧化二钒在高温下发生置换反应生成V,根据反应物、生成物及反应条件书写方程式;
(2)反应过程中元素化合价变化的为氧化还原反应,反应①发生的反应是亚硫酸钠具有还原性,能将V2O5还原为VOSO4,操作1、操作2是过滤操作,据此判断用到的玻璃仪器;
(3)该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,铵根离子和VO3-反应生成难溶性的NH4VO3,根据图知,在80℃时沉降率最,图象可知沉钒率在80°C最高;
(4)NH4VO3在焙烧变化的图象和质量变化分析判断,根据NH4VO3在焙烧变化的图象可知:
2NH4VO3═V2O5+2NH3↑+H2O
234g 34g 18g
减少值开始为0~17g,曲线到200℃时(约为16.0g)曲线开始平直;到约为300℃时又开始减少(H2O的质量),到350℃时减少24g时就不再变化;
(5)电池充电时阳极上VO2+失电子发生氧化反应;
解答 解:(1)工业由V2O5冶炼金属钒常用铝热剂法,铝和五氧化二钒在高温下发生置换反应生成V,根据反应物、生成物及反应条件知,该反应方程式为3V2O5+10Al$\frac{\underline{\;高温\;}}{\;}$5Al2O3+6V,
故答案为:3V2O5+10Al$\frac{\underline{\;高温\;}}{\;}$5Al2O3+6V;
(2)反应①、②、③、④中,反应①是向滤渣中加入亚硫酸钠和稀硫酸,亚硫酸钠具有还原性,能将V2O5还原为VOSO4,反应②发生氧化还原反应的是将两部分滤液混合并加入氯酸钾,氯酸钾具有氧化性,能将VOSO4氧化为(VO2)2SO4,为氧化还原反应,反应③调节溶液pH为8且采用离子交换方法得到VO3-,向溶液中加入氯化铵,得到难溶性的NH4VO3,属于复分解反应,反应④是焙烧NH4VO3得到V2O5,元素化合价未变不是氧化还原反应,氧化还原反应为①②,反应①的离子方程式为:V2O5+SO32-+4H+=2VO2++SO42-+2H2O,操作1、操作2是过滤操作,用到的玻璃仪器是:烧杯、玻璃棒、漏斗,
故答案为:①②;V2O5+SO32-+4H+=2VO2++SO42-+2H2O;烧杯、玻璃棒、漏斗;
(3)该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,铵根离子和VO3-反应生成难溶性的NH4VO3,离子方程式为NH4++VO3-=NH4VO3↓,根据图知,在80℃时沉降率最大,控制温度的方法是:将反应容器置于80℃的水浴中,
故答案为:将反应容器置于80℃的水浴中;
(4)根据NH4VO3在焙烧变化的图象可知:
2NH4VO3═V2O5+2NH3↑+H2O
234g 34g 18g
减少值开始为0~17g,曲线到200℃时(约为16.0g)曲线开始平直;到约为300℃时又开始减少(H2O的质量),到350℃时减少24g时就不再变化,所以NH4VO3在焙烧过程中200℃时左右先失去氨生成HVO3;HVO3在300~350℃再失去水生成V2O5,反应的化学方程式为:2HVO3$\frac{\underline{\;300°C-350°C\;}}{\;}$V2O5+H2O,
故答案为:2HVO3$\frac{\underline{\;300°C-350°C\;}}{\;}$V2O5+H2O
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为VO2++V2++2H+$?_{充电}^{放电}$VO2++H2O+V3+.电池充电时阳极上VO2+失电子发生氧化反应,电极反应式为VO2++H2O-e-=VO2++2H+,
故答案为:VO2++H2O-e-=VO2++2H+.
点评 本题考查物质的分离和提纯,为高频考点,侧重考查氧化还原反应、离子反应方程式的书写、原电池和电解池原理等知识点,明确反应原理是解本题关键,知道流程图中发生的反应及实验基本操作,难点是电极反应式的书写,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 0.8 mol•L-1 | B. | 1.6 mol•L-1 | C. | 1.4 mol•L-1 | D. | 0.75 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z | W |
| A. | 金属性由强到弱的顺序为:Z、W | |
| B. | 原子半径由大到小的顺序为:Y、Z | |
| C. | 简单气态氢化物的稳定性由强到弱的顺序:X、Y | |
| D. | 工业上常用电解熔融Z的氧化物得到单质Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时Pb为负极,此时溶液中的SO42-向Pb电极迁移 | |
| B. | 铅蓄电池电解CuCl2溶液,若制得2.24LCl2(标准状况),这时电池内消耗的H2SO4至少0.2mol | |
| C. | 放电完全后铅蓄电池可进行充电,此时铅蓄电池的负极连接外电源的正极上 | |
| D. | 充电时阳极的电极反应式:PbSO4+2H2O-2e-=PbO2+4H++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 序号 | t/h | t/℃ | m/g | x |
| 1 | 3 | 80 | 5 | 4 |
| 2 | 3 | 160 | 10 | 1 |
| 3 | 4 | 160 | 10 | 0.8 |
| 4 | 4 | 160 | 5 | 0 |
| 5 | 5 | 80 | 5 | 3 |
| 6 | 5 | 160 | 15 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
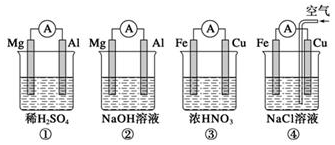
| A. | ①②中Mg作负极,③④中Fe作负极 | |
| B. | ②中Mg作正极,电极反应式为6H2O+6e-═6OH-+3H2↑ | |
| C. | ③中Fe作负极,电极反应式为Fe-2e-═Fe2+ | |
| D. | ④中Cu作正极,电极反应式为2Cl-+2e-=Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
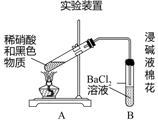 | 现象 1A试管中黑色沉淀逐渐溶解 2A试管内上方出现浅红棕色气体 3B试管中出现白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com