
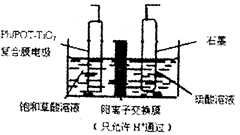
| A.电解时石墨电极应与直流电源的正极相连 |
| B.阴极反应式为:HOOCCOOH+2H++2e-=OHCCOOH+H2O |
| C.电解时石墨电极上有O2放出 |
| D.电解一段时间后,硫酸溶液的pH不变化 |
科目:高中化学 来源:不详 题型:单选题
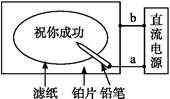
| A.铅笔端作阳极,发生还原反应 |
| B.铂片端作阴极,发生氧化反应 |
| C.铅笔端有少量的氯气产生 |
| D.a点是负极,b点是正极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
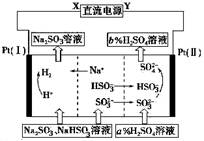
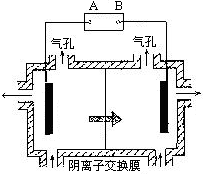
| A.X为直流电源的负极,Y为直流电源的正极 |
| B.阳极区pH增大 |
| C.图中的b>a |
| D.该过程中的产品主要为H2SO4和H2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电路中共转移0.9 mol电子 |
| B.阳极得到的气体中有O2,且其物质的量为0.35 mol |
| C.阴极的质量增加3.2 g |
| D.铝元素仅以Al(OH)3的形式存在 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用铜片连接电源的正极,另一电极用铂片 |
| B.用碳棒连接电源的正极,另一电极用铜片 |
| C.用氢氧化钠溶液吸收阴极产物 |
| D.用带火星的木条检验阳极产物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Cr2O3)冶炼铬的工艺流程如下:
Cr2O3)冶炼铬的工艺流程如下: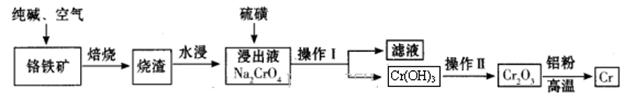
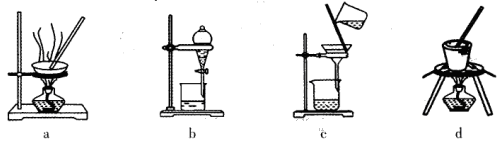
 Cr2O72-+H2O)。
Cr2O72-+H2O)。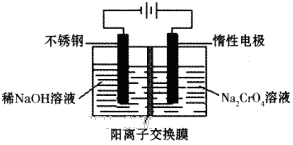
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
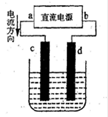
| A.电镀前,铁皮可用热碱溶液除油渍,盐酸除铁锈 |
| B.c为铁,d为锌 |
| C.用含Zn2+的盐配成电解质溶液 |
| D.电镀时,发生氧化和还原反应的都是锌元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
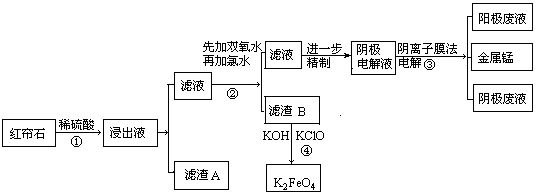
| 离子 | Fe3+ | Al3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀的pH | 2.7 | 3.7 | 7.0 | 7.8 | 9.3 |
| 完全沉淀的pH | 3.7 | 4.7 | 9.6 | 9.8 | 10.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com