
【题目】通常将 称作标准状况,标准状况下的气体摩尔体积约为 ,若标准状况下CO和CO2混合气体的密度为1.607g/L,则混合气体的平均相对分子质量为 ;其中CO的质量分数为 ;若将0.1mol该混合气体通入含0.1molCa(OH)2的澄清石灰水中,写出反应的离子方程式: 。
科目:高中化学 来源: 题型:
【题目】现有下列九种物质:① H2 ② 铝 ③ CuO ④ CO2 ⑤ NaHSO4 ⑥ Ba(OH)2固体 ⑦ 氨水 ⑧ 稀硝酸 ⑨ 熔融Al2(SO4)3。
(1)上述状态下可导电的是____________;属于电解质的是____________;属于非电解质的是______________。(填序号)
(2)写出⑤、⑨在水中的电离方程式 、 。
(3)34.2 g ⑨溶于水配成250 mL溶液,SO![]() 的物质的量浓度为___________。
的物质的量浓度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K下,将1mol蔗糖溶解在1L水中,此溶解过程中体系的G = H-TS和S的变化情况是
A. G>0,S<0 B. G<0,S>0 C. G>0,S>0 D. G<0,S<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液。观察到的现象是先出现黄色沉淀,最终出现黑色沉淀。已知有关物质的溶度积Ksp (25 ℃)如下:
AgCl | AgI | Ag2S | |
Ksp | 1.8×10-10 | 8.51×10-16 | 6.3×10-50 |
下列叙述错误的是
A.沉淀转化的实质就是沉淀溶解平衡的移动
B.溶解度小的沉淀可以转化为溶解度更小的沉淀
C.AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同
D.25 ℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方法能达到实验目的的是
A. 用淀粉溶液检验溶液中是否存在碘单质
B. 用分液漏斗分离水与乙醇的混合物
C. 用氯化钡溶液鉴别碳酸钠溶液与硫酸钠溶液
D. 用排水集气法收集氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白藜芦醇(C14H12O3)是一种天然的肿瘤化学预防剂,来源于花生、葡萄和桑葚等植物。该物质属于
A. 无机物 B. 有机物 C. 单质 D. 氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)46 g NO2和N2O4的混合气体其分子数最多接近____________,氧原子数目为____________。
(2)气体化合物A分子式可表示为OxFy,已知同温同压下10 mL A受热分解生成15 mL O2和10 mL F2,则A的化学式为____________,推断的依据为______________________。(填写定律的名称)
(3)有NaCl、CaCl2、AlCl3三种溶液,分别与足量的AgNO3溶液反应:
①若所含溶质的物质的量相等,则生成沉淀的物质的量之比是________________;②若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量之比_____________。
(4)现将200mL0.01mol/LNaOH与50mL某浓度的Ca(OH)2溶液混合(混合后体积变化忽略不计),所得溶液中OH-的物质的量浓度是0.016mol/L,则Ca(OH)2溶液的物质的量浓度是 mol/L。
(5)现有标况下VL某气体,它由双原子分子构成,它的摩尔质量为Mg·mol-1。若阿伏加德罗常数用NA表示,则:
①该气体所含原子数为____________。
②该气体溶于1L水中(不考虑反应),若所得的溶液的密度为d g·cm-3,其溶液中溶质的物质的量浓度为______ _ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在VL密闭容器中,A、B、C三种物质的物质的量随时间变化的曲线如图所示,由图中数据分析:
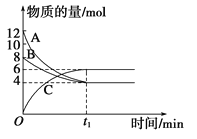
(1)反应的化学方程式为_______________。
(2)从开始到t1 min末时,用物质C表示的反应速率为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com