
分析 (1)根据化合价代数和为0,分析解答;
(2)反应2 LiBH4+2 HCl$\frac{\underline{\;-80℃\;}}{\;}$2 LiCl+B2H6+2H2中,氯化氢是氧化剂,B2H6中的部分氢元素失电子是还原剂,由反应可知2mol完全反应转移2mol的电子,由此分析解答.
解答 解:(1)因为LiBH4和B2H6中的氢元素均显-1价,而Li是+1价,所以LiBH4中硼元素的化合价为+3价,故答案为:+3;
(2)反应2 LiBH4+2 HCl$\frac{\underline{\;-80℃\;}}{\;}$2 LiCl+B2H6+2H2中,氯化氢是氧化剂,B2H6中的部分氢元素失电子是还原剂,由反应可知2mol完全反应转移2mol的电子,所以4 mol LiBH4完全反应后共失去4mol的电子,故答案为:B2H6;4.
点评 本题考查氧化还原反应,题目难度中等,把握元素化合价的判断方法,从化合价变化的角度分析氧化还原反应.


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:选择题
| A. | 滴定管装滴定液时不应先用滴定液润洗 | |
| B. | 锥形瓶用作反应容器时一定不能加热 | |
| C. | 蒸馏时温度计水银球可以高于蒸馏瓶支管口 | |
| D. | 振荡分液漏斗时应关闭其玻璃塞和活塞 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
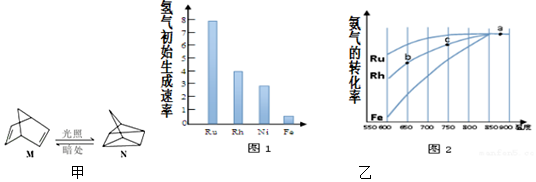
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:K2FeO4<O2 | |
| B. | K2FeO4可用作自来水的消毒剂和净水剂 | |
| C. | K2FeO4可用作碱性K2FeO4-Zn电池的负极材料 | |
| D. | 常温常压下,该反应每生成22.4L O2,转移电子的数目为4×6.02×1023个 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验操作和现象 | 结论 |
| A | 室温下,向苯酚钠溶液中通入足量CO2,溶液变浑浊 | 碳酸的酸性比苯酚的强 |
| B | 向某溶液中滴加氯水后再加入KSCN溶液,溶液呈红色 | 溶液中一定含有Fe2+ |
| C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 | Fe3+的氧化性比I2的强 |
| D | 取少量食盐溶于水,加稀硫酸酸化,再滴入淀粉溶液,溶液未呈蓝色 | 该食盐中不含有碘酸钾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com