
碳酸钠和碳酸氢钠是生活中常见的物质。请回答下列问题。
(1)碳酸氢钠的化学式是 ,俗称 。
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为 。等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者 后者(填“>”、“<”或“=”)。
(3)除去碳酸钠固体中碳酸氢钠的反应的化学方程式为 。
(1)NaHCO3 ;小苏打 (2)HCO3- + H+ = H2O + CO2↑;=
(3)2NaHCO3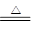 Na2CO3
+ H2O + CO2↑
Na2CO3
+ H2O + CO2↑
【解析】
试题分析:1)碳酸氢钠的化学式是NaHCO3,俗称小苏打。
(2)碳酸氢钠能和氢离子反应,所以碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为HCO3- + H+ = H2O + CO2↑;根据碳酸氢钠和碳酸钠的化学式NaHCO3、Na2CO3并依据碳原子守恒可知,等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者=后者。
(3)碳酸氢钠稳定性差,受热易分解生成碳酸钠、水和CO2,所以除去碳酸钠固体中碳酸氢钠的方法是加热,反应的化学化学方程式为2NaHCO3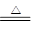 Na2CO3 + H2O
+ CO2↑。
Na2CO3 + H2O
+ CO2↑。
考点:考查碳酸氢钠的性质、用途、俗名、物质的分离与提纯、碳酸钠、碳酸氢钠与盐酸反应的计算、方程式的书写等
点评:该题是基础性试题的考查,难度不大。主要是考查学生对碳酸氢钠性质、用途等则知识的熟悉了解程度,意在培养学生灵活运用基础知识解决实际问题的能力,有利于培养学生的规范答题能力。


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源:四川省广元中学2010届高三第四次月考、化学试卷 题型:058
我国著名化学家侯德榜先生发明的“侯氏制碱法”,因原料利用率高,并能进行连续生产,从而享誉中内外.“侯氏制碱法”的基本做法是向饱和食盐水中通入氨气和二氧化碳,获得碳酸氢钠晶体,再将所得碳酸氢钠晶体加热分解后即可得到纯碱.它的反应原理可用下列化学方程式表示:
NaCl(饱和)+NH3+CO2+H2O=NaHCO3↓+NH4Cl
2NaHCO3Na2![]() CO3+CO2+H2O
CO3+CO2+H2O
某课外兴趣小组同学,按照“侯氏制碱法”原理,设计了如下一套实验装置

实验室可选药品有浓氨水、纯碱、大理石、稀盐酸、稀硫酸、熟石灰、氯化铵、氯化钠
(1)选用最合适的试剂的名称D________
(2)本实验具体操作过程中,应先通________气体,再通________气体;
(3)指出该装置的三处错误________ ________ ________
(4)在改进装置后,该同学进行了实验,实验所用的饱和NaCl溶液中含溶质58.5 g,实验最后得到无水碳酸钠26 g,则其产率为________;该同学针对其实验结果,认真分析了造成损失的原因,发现其操作步骤并没有错误,则主要原因是________
(5)在“侯氏制碱法”的工业生产中,原料的利用率高,大大降低了成本.请问本实验中哪些物质可重复利用?________
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源:同步题 题型:实验题
 Na2CO3+CO2↑+H2O。某课外兴趣小组同学,按照“侯氏制碱法”原理,设计了如图所示的一套实验装置:
Na2CO3+CO2↑+H2O。某课外兴趣小组同学,按照“侯氏制碱法”原理,设计了如图所示的一套实验装置: 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com