
| A. | 对废气、废水、废渣进行严格处理 | |
| B. | 在化工生产中少用或不用有害物质以及少排放或不排放有害物质 | |
| C. | 在化工生产中,不使用任何化学物质 | |
| D. | 在化工厂种草种树,使其成为花园式工厂 |
分析 根据绿色化学的核心和特点判断,其核心是要从源头上杜绝污染,特点是:
(1)充分利用资源和能源,采用无毒无害的原料;
(2)在无毒无害的条件下进行反应,以减少向环境排放废物;
(3)提高原子利用率,力图使原料的原子都被产品所消纳,实现零排放;
(4)生产出有利于环境保护、社区安全和人体健康的环境友好产品.
解答 解:A.对废气、废水、废渣进行严格处理,不是从源头上减少或消除化学工业对环境的污染,故A错误;
B.在化工生产中少用或不用有害物质以及少排放或不排放有害物质,符号绿色化学的理念,故B正确;
C.自然界的所有物质都是化学物质,故C错误;
D.在化工厂种草种树,使其成为花园式工厂只是环境的绿化,与绿色化学无关,故D错误;
故选B.
点评 本题考查绿色化学,注意其核心即可解答,明确保护好环境,就要了解环境的污染源和防治措施,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | VIIA族元素的非金属性:F>Cl,所以VIIA族元素氢化物的酸性:HF>HCl | |
| B. | 第二周期元素氢化物稳定性:HF>H2O,所以第三周期元素氢化物稳定性:HCl>H2S | |
| C. | 第二周期主族元素最外层电子数从1递增至7,所以第二周期主族元素的最高化合价也从+1递增至+7 | |
| D. | 工业制取金属钾的反应为:KCl (1)+Na (1)$\frac{\underline{\;850℃\;}}{\;}$NaCl(1)+K(g),所以金属性:Na>K |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
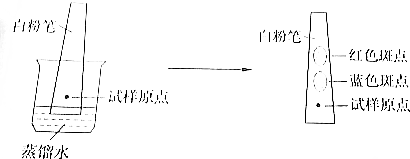
| A. | 是固定相 | B. | 是流动相 | ||
| C. | 是惰性支持物 | D. | 既是固定相,又是流动相 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
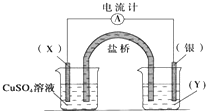 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (c-a-b)kJ | B. | (a+b-c)kJ | C. | (2c-a-b)kJ | D. | (2c-a-b)/2 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
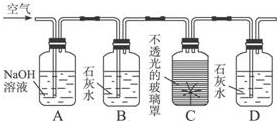
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
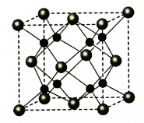
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K3C60的摩尔质量是837 | |
| B. | 1 mol K3C60中含有的离子数目为63×6.02×1023 | |
| C. | 该晶体在熔融状态下能导电 | |
| D. | 该物质的化学式可写为KC20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com