
【题目】某种“光敏性高分子”材料在荧光屏及大规模集成电路中应用广泛。其结构如下,对该“光敏性高分子”,下列叙述正确的是( )

A.化学式为(C11H11O2)n
B.它能发生加成反应,不能发生水解反应
C.它可以和FeCl3溶液发生显色反应
D.1mol该分子最多能和4n mol H2发生加成反应
 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】芬顿( Fenton )试例,成分为双氧水和亚铁盐,需要酸性环境。电-Fenton法是用于水体里有机污染物降解的高级氧化技术。其反应原理如图2所示.其中电解产生的H2O2与Fe2+发生Fenton反应:Fe2++H2O2=Fe3++OH-+·OH,生成的羟基自由基(·OH)对有机物有极强的氧化能力。下列说法正确的是

A.a极是电源的正极
B.电解池中只有O2、Fe3+发生还原反应
C.阳极上发生电极反应:H2O-e-=·OH+H+
D.消耗1molO2,可以产生2mol·OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修22:化学生活与技术]氯碱工业过程中产生了大量的盐泥。某氯碱工厂的盐泥组成如下:
成分 | NaCl | Mg(OH)2 | CaCO3 | BaSO4 | SiO2等不溶于酸的物质 |
质量分数(%) | 15~20 | 15~20 | 5~10 | 30~40 | 10~15 |
该工厂进一步利用盐泥生产了七水硫酸镁,设计了工艺流程如图:

回答下列问题:
(1)反应器中加入酸溶解,反应液控制pH为5左右,反应温度在50℃左右,写出有关化学反应方程式 。
(2)在滤饼中检测到硫酸钙的成分,其原因是 。
(3)已知一些盐的溶解度如下图。在滤液I中通入高温水蒸气进行蒸发结晶,为了析出晶体I,应控制温度在__________℃。

(4)步骤II操作是_______________,
(5)步骤III在工业上常用的设备是______________(填字母)。
A.加压干燥器 B.蒸馏塔 C.离心机 D.真空干燥器
(6)准确称取制备产品ag,将其加入到盛有V1mL c1mol/L的NaOH溶液的锥形瓶中,溶解后,加入酚酞溶液2滴,溶液变红色,再用c2mol/L的盐酸进行滴定,消耗盐酸V2mL,则样品MgSO4·7H2O的质量分数是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是人类生活中继铜、铁之后又一个重要的金属。工业上冶炼金属铝的原料来源于自然界中重要的矿物质钒土(主要成分:Al2O3;还有SiO2、Fe2O3、FeCO3、MgCO3等杂质)。从钒土中提取得到Al2O3的工艺流程如下图所示:

请回答下列问题:
(1)固体A所含物质的化学式(或分子式)是 。
(2)写出溶液A与足量气体B反应的离子方程式 。
(3)工业冶炼金属铝通常用石墨碳块作电解槽的阳极,请你根据电解原理解释电解冶炼铝的过程中,需要定期补充阳极碳块的原因 。
(4)Al2O3的熔点很高,因而在工业冶炼时,需将Al2O3熔于熔化的冰晶石(Na3AlF6)中进行电解。请写出电解过程中阴极的电极反应式 。工业上通常将Al(OH)3和Na2CO3一同溶于氢氟酸来制取冰晶石,反应时放出CO2气体,写出该反应的化学方程式 。
(5)有一位同学查阅资料发现,AlCl3的熔点很低。他提出:可通过电解熔融状态的AlCl3制取金属铝。你认为他提出的方案是否可行?为什么? 。
(6)某企业用上述工艺流程进行生产,每10.0t钒土可得到金属铝1.35t。如果不考虑生产过程的损耗,请你计算钒土中Al2O3的质量分数 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸在化学工业中有着极其广泛的应用。
(1)将1.25 mol的NO、NO2、N2O4混合物(其中NO的体积分数为0.60)通入水中,在空气充足的条件下完全反应后可获得硝酸的物质的量范围是_______________。
(2)向稀硝酸中加入18.4 mol/L的浓硫酸(98%)作吸水剂并蒸馏得浓硝酸,当其浓度下降到87%(密度1.8 g/cm3)以下时,则失去吸水能力。50 mL 18.4 mol/L的浓硫酸作为吸水剂时,最多可吸水__ g。
(3)在65%的HNO3(质量m1)中加入72%的Mg(NO3)2(质量m2)后蒸馏,分别得到97.5%的HNO3和60%的Mg(NO3)2溶液(其中不含硝酸)。若蒸馏过程中,硝酸、硝酸镁均无损耗,H2O的损耗占总质量的5%,则蒸馏前投料比![]() =______________。
=______________。
(4)硝酸工业中的尾气用烧碱进行吸收产物为NaNO2、NaNO3和H2O。现有含0.50mol氮氧化物的尾气,恰好被一定量的NaOH溶液完全吸收。已知反应后溶液含有0.35molNaNO2。若将尾气NO和NO2的平均组成用NOx表示,则x = 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图有机物分子中带“※”碳原子是手性碳原子(连有四个不同基团的碳原子)。该有机物分别发生下列反应,生成的有机物分子中不会含有手性碳原子的是( )

①与甲酸发生酯化反应
②与足量NaOH水溶液反应
③与银氨溶液作用只发生银镜反应
④催化剂作用下与H2反应
A. ①②③④ B. ①③
C. ②④ D. 以上反应都不成立
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向体积恒定为2 L的密闭容器里充入2 mol M和一定量的N,发生如下反应:M(g)+N(g)![]() E(g)。当反应进行到4min时达到平衡,测得M的浓度为0.2 mol·L-1。下列说法正确的是( )
E(g)。当反应进行到4min时达到平衡,测得M的浓度为0.2 mol·L-1。下列说法正确的是( )
A.4min时,M的转化率为80%
B.4min时,用M表示的反应速率为0.8mol·L-1·min-1
C.4min后,向容器中充入不参与反应的稀有气体,M的物质的量减小
D.2min时,M的物质的量浓度为0.6mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯的同系物是人类最早认识的芳香族化合物,其中对二甲苯(英文名称p—xylene,缩写为PX)是化学工业的重要原料。
已知: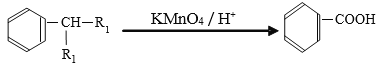
(1)写出PX的结构简式______________。
(2)PX可能发生的反应有__________、_____________。(填反应类型,只填两种。)
(3)有机物M存在如下图所示的转化关系,其中A 是PX的一种同分异构体。

已知:M的分子式为C16H22O4,D能发生银镜反应。
①B的苯环上存在3 种不同化学环境的氢原子,则B 的结构简式是__________。
②D分子中所含的官能团是______________(填化学式)。
③M的结构简式是_______________。
(4)F是B的一种同分异构体,具有如下特征:
a.是苯的对位二取代物; b.遇FeCl3溶液显示紫色; c.能与碳酸氢钠溶液反应。
写出F与NaHCO3溶液反应的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M是一种常用香料的主要成分之一,其合成路线如下。
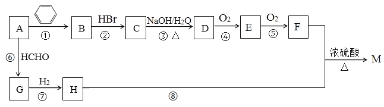
已知:
①相同条件下1体积烃A完全燃烧消耗4体积氧气;
②RC≡CH+HCHO![]() RC≡CCH2OH;
RC≡CCH2OH;
③反应①的原子利用率为100%,反应类型属于加成反应;
④M的分子式为C13H18O2。
回答下列问题:
(1)A的名称为___________;G分子中有___ _个碳原子在同一条直线上。
(2)反应②~⑧中属于加成反应的是______;H中官能团的名称为___________。
(3)物质M的结构简式为____________。B的一种同类别异构体存在顺反异构,该物质发生加聚反应生成的高分子化合物的结构简式为_____________。
(4)反应③的化学反应方程式为_______________。
(5)符合下列条件的F的同分异构体共有_____种。
①能发生银镜反应;②能发生水解反应;③属于芳香族化合物。
其中核磁共振氢谱为4组峰,且峰面积之比为6∶2∶1∶1的为 (任写一种物质的结构简式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com