
常温下,有浓度均为1 mol·L-1的下列4种溶液:
①H2SO4溶液 ②NaHCO3溶液 ③NH4Cl溶液 ④NaOH溶液
(1)这4种溶液pH由大到小的顺序是 ,其中由水电离的H+浓度最小的是 。(均填序号)
(2)②中各离子浓度由大到小的顺序是 ,NaHCO3的水解平衡常数Kh= mol·L-1。(已知碳酸的电离常数K1=4×10-7,K2=5.6×10-11)
(3)向③中通入少量氨气,此时 的值 (填“增大”、“减小”或“不变”)。
的值 (填“增大”、“减小”或“不变”)。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积 ④的体积(填“大于”、“小于”或“等于”之一)。
(1)(2分) ④②③① ①
(2)(4分)c(Na+)>c(HCO3—)>c(OH—)>c(H+)>c(CO32—) 2.5×10—8
(3)(1分)减小 (4)(1分)大于
解析试题分析:(1)硫酸是二元强酸,溶液显强酸性;碳酸氢钠溶液中HCO3-的水解程度强于HCO3-的电离程度,溶液显弱碱性;氯化铵溶于水NH4+水解,溶液显弱酸性;氢氧化钠是强碱,溶于水显强碱性,所以这4种溶液pH由大到小的顺序是④②③①;水是弱电解质,存在电离平衡H2O H++OH-。因此酸电离出的氢离子浓度或碱电离出的OH-浓度越大,对水的电离抑制程度越大。硫酸中氢离子浓度大于氢氧化钠溶液中OH-浓度,所以硫酸溶液中由水电离的H+浓度最小,答案选①。
H++OH-。因此酸电离出的氢离子浓度或碱电离出的OH-浓度越大,对水的电离抑制程度越大。硫酸中氢离子浓度大于氢氧化钠溶液中OH-浓度,所以硫酸溶液中由水电离的H+浓度最小,答案选①。
(2)由于碳酸氢钠溶液中HCO3-的水解程度强于HCO3-的电离程度,溶液显弱碱性,所以溶液中各离子浓度由大到小的顺序是c(Na+)>c(HCO3—)>c(OH—)>c(H+)>c(CO32—);根据水解方程式HCO3- H2CO3+OH-可知,碳酸氢钠的水解常数Kh=
H2CO3+OH-可知,碳酸氢钠的水解常数Kh=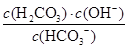 =
=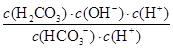 =
= =
= =2.5×10—8 mol·L-1。
=2.5×10—8 mol·L-1。
(3)氯化铵中存在水解平衡NH4++H2O NH3·H2O+H+,向溶液中通入少量氨气,平衡向正反应方向越大,因此溶液中
NH3·H2O+H+,向溶液中通入少量氨气,平衡向正反应方向越大,因此溶液中 的值减小。
的值减小。
(4)如果NH4Cl溶液和NaOH溶液等浓度、等体积混合后生成氯化钠和一水合氨,溶液显碱性。要使溶液显中性,则氯化铵应该是过量的,所以混合前③的体积大于④的体积。
考点:考查溶液酸碱性比较、水的电离、盐类水解、溶液中离子浓度大小比较以及水解常数计算


科目:高中化学 来源: 题型:填空题
(1)将等质量的Zn粉分别投入:a:10 mL 0.1 mol·L-1 HCl和
b:10 mL 0.1 mol·L-1醋酸中。(填“>”、“=”或“<”)
①若Zn不足量,则反应速率a b,
②若Zn过量,产生H2的量a b。
(2)将等质量的Zn粉分别投入pH=1,体积均为10 mL的a:盐酸b:醋酸中
①若Zn不足量,则起始反应速率a b,
②若Zn过量,产生H2的量a b。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某学生欲用已知物质的量浓度的醋酸来测定未知物质的量浓度的氢氧化钠溶液时,选择适当的指示剂。请填写下列空白:
(1)用标准醋酸滴定待测的氢氧化钠溶液时,从下列选项中选出最恰当的一项________。
| | 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 |
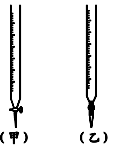
| A | 碱 | 酸 | 石蕊 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 酚酞 | (甲) |
| D | 酸 | 碱 | 石蕊 | (乙) |
| | 待测氢氧化钠 | 0.100mol/L醋酸的体积 | |
| 滴定次数 | 溶液的体积(ml) | 滴定前的刻度(ml) | 滴定后的刻度(ml) |
| 第一次 | 25.00 | 0.00 | 24.98 |
| 第二次 | 25.00 | 1.56 | 27.86 |
| 第三次 | 25.00 | 0.22 | 25.24 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知H2A在水中存在以下平衡:H2A H++HA-,HA-
H++HA-,HA- H++A2-。回答以下问题:
H++A2-。回答以下问题:
(1)已知常温下,H2A的钙盐(CaA)饱和溶液中存在平衡:
CaA(s) Ca2+(aq)+A2-(aq) ΔH > 0。
Ca2+(aq)+A2-(aq) ΔH > 0。
①温度升高时,Ksp________(填“增大”、“减小”或“不变”下同)。
②滴加少量浓盐酸,c (Ca2+)________,原因是____ ______________(用文字和离子方程式说明)。
(2)若向CaA悬浊液中加入CuSO4溶液,生成一种黑色固体物质,写出该过程中反应的离子方程式______________________。若某CuSO4溶液中c (Cu2+)=0.02 mol/L,如果要生成Cu(OH)2沉淀,应调整溶液pH,使之大于________(已知Ksp[Cu(OH)2]=2.0×10-20)。
(3)常温下,向某纯碱溶液中滴入酚酞,溶液呈红色,则该溶液呈________性。在分析该溶液遇酚酞呈红色的原因时,甲同学认为是配制溶液时所用的纯碱样品中混有NaOH所致;乙同学认为是溶液中电离出的CO32-水解所致,请你设计一个简单的实验方案给甲和乙两位同学的说法进行评判(包括简要操作、现象和结论)_________________ ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)室温下在pH=12的NaCN溶液中,由水电离的c(OH—)为 mol?L—1。
(2)浓度为0.1mol?L—1的下列各物质的溶液中,c(NH4+)由大到小的顺序是___(填序号)。
①NH4Cl ②NH4HSO4 ③NH3?H2O ④CH3COONH4
(3)某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A=H+ +HA—,HAˉ H+ +A2—。
H+ +A2—。
①则Na2A溶液显____性;NaHA溶液显 性(填“酸性”、“中性”或“碱性”)。
②若有0.1mo1?L—1Na2A的溶液,其中各种离子浓度由大到小的顺序是: (填序号)。
| A.c(Na+)>c(A2—)>c(OH—)>c(HA—)>c(H+) |
| B.c(Na+)> c(OH—)>c(HA—)> >c(A2—) > c(H+) |
| C.c(Na+)> c(H+)> c(A2—)> c(OH—)>c(HA—) |
| D.c(A2—)>c(Na+)> c(OH—) > c(H+)>c(HA—) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
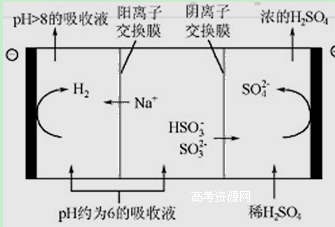
(8分)最近雾霾天气又开始肆虐我国大部分地区。其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2。
(1)钠碱循环法中,吸收液为Na2SO3溶液,该吸收反应的离子方程式是
(2)已知H2SO3的电离常数为 K1=1.54×10-2 , K2=1.02×10-7, H2CO3的电离常数为 K1=4.30×10-7, K2= 5.60×10-11,则下列微粒可以共存的是_____________。
A.CO32- HSO3- B.HCO3- HSO3-
C.SO32- HCO3- D.H2SO3 HCO3-
(3)吸收液吸收SO2的过程中,pH随n(SO3²﹣):n(HSO3﹣)变化关系如下表:
| n(SO3²﹣):n(HSO3﹣) | 91 :9 | 1 :1 | 1 :91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
常温下有0. 1 mol/L的以下几种溶液,①H2SO4溶液②NaHSO4溶液③CH3COOH溶液④HCl溶液⑤HCN溶液⑥NH3·H2O,其中如下几种溶液的电离度(即已经电离的占原来总的百分数)如下表(已知H2SO4的第一步电离是完全的),回答下面问题:
| ①H2SO4溶液HSO4- | ②NaHSO4溶液HSO4- | ③CH3COOH | ④HCl溶液 |
| 10% | 29% | 1.33% | 100% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
从海水中提取镁是世界各国获得镁的主要来源,以下是制取镁的过程中涉及的几种物质的溶度积,根据你所学的知识回答下列几个问题:
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 |
| 溶度积 | 2.8×10–9 | 6.8×10–6 | 5.5×10–6 | 1.8×10–11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com