
【题目】下列实验现象预测正确的是( )
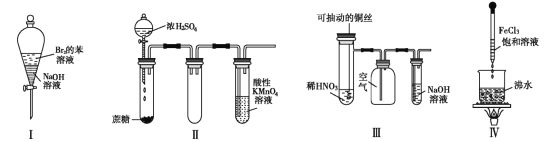
A. 实验Ⅰ:振荡后静置,上层溶液颜色保持不变
B. 实验Ⅱ :酸性 KMnO4 溶液中出现气泡,且颜色逐渐褪去
C. 实验Ⅲ:微热稀 HNO3 片刻,溶液中有气泡产生,广口瓶内始终保持无色
D. 实验Ⅳ:滴入 FeCl3 后,可形成带电的胶体,该分散系导电能力增强
【答案】B
【解析】A.根据单质溴能与NaOH溶液发生反应,苯与水互不相溶;B.根据浓硫酸具有脱水性和氧化性的性质分析;C.根据在加热时稀硝酸与铜发生反应,硝酸被还原成NO,广口瓶内有空气,可与NO反应;D.胶体粒子带电荷,胶体本身不带电。
A项,苯的密度比水小,位于上层,苯中的Br2与NaOH溶液发生反应,因此振荡后静置,上层溶液褪色,故A项错误;
B项,浓H2SO4与蔗糖发生氧化还原反应生成SO2和CO2,CO2不与酸性KMnO4溶液反应,有气泡产生,SO2与酸性KMnO4溶液发生氧化还原反应使溶液褪色,故B项正确;
C项,微热稀HNO3片刻,铜与稀HNO3发生反应生成NO,NO与广口瓶内的O2反应生成红棕色的NO2,故C项错误。
D项,FeCl3饱和溶液滴入沸水中继续煮沸至红褐色,生成氢氧化铁胶体,胶体电中性,不带电,故D项错误;
综上所述,本题正确答案为B。


科目:高中化学 来源: 题型:
【题目】某学生为了探究影响化学反应速率的外界因素,进行以下实验。
(1)向100mL稀硫酸中加入过量的锌粉,标准状况下测得数据累计值如下:
时间/min | 1 | 2 | 3 | 4 | 5 |
氢气体积/mL | 50 | 120 | 232 | 290 | 310 |
①在0~1、1~2、2~3、3~4、4~5min各时间段中:
反应速率最大的时间段是________min,主要的原因可能是_____________________;
反应速率最小的时间段是________min,主要的原因可能是_____________________。
②为了减缓反应速率但不减少产生氢气的量,可以在稀硫酸中加入________(填序号)。
a.蒸馏水 b.NaOH溶液 c.NaNO3溶液 d.Na2CO3溶液
(2)进行以下对比实验并记录实验现象。
实验 Ⅰ
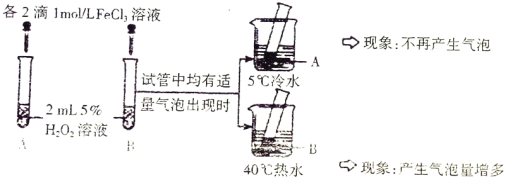
实验 Ⅱ:另取两支试管分别加入5mL5%eH2O2溶液和5mL10%H2O2溶液,均未观察到有明显的气泡
产生。
①双氧水分解的化学方程式是________________。
②实验 Ⅰ 的目的是______________。
③实验 Ⅱ 未观察到预期现象,为了达到该实验的目的,可采取的改进措施是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列的分离方法不正确的是 ( )
A.用酒精萃取碘水中的碘B.用淘洗的方法从沙里淘金
C.用蒸馏的方法将自来水制成蒸馏水D.用过滤的方法除去食盐水中的泥沙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉和纤维素是常见的多糖,在一定条件下它们都可以水解生成葡萄糖。
(1)淀粉在浓硫酸作用下水解生成葡萄糖的化学方程式为___________。
(2)某学生设计了如下实验方案用以检验淀粉水解的情况:
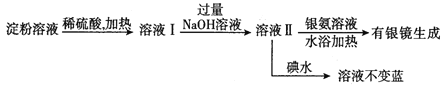
下列结论正确的是_______。
A.淀粉尚有部分未水解 B.淀粉已完全水解
C.淀粉没有水解 D.淀粉已水解,但不知是否完全水解
(3)一种测定饮料中糖类物质含量(所有糖类物质以葡葡糖计算)的方法如下:
取某无色饮料20.00mL加入稀硫酸煮沸,充分反应后,冷却,加入适量的氢氧化钠溶液并稀释至100.00mL。取10.00mL稀释液,加入30.00mL0.0150mol/L标准溶液,置于暗处15分钟。然后滴加2~3滴淀粉溶液作指示剂,再用0.01200mol/LNa2S2O3标准溶液滴定反应所剩余的I2,当溶液由蓝色变为无色且半分钟不变时,反应达到终点,共消耗Na2S2O3标推溶液25.00mL。己知:
a.I2在碱性条件下能与萄萄糖反应:C6H12O6+I2+3NaOH=C6H11O7Na+2NaI+2H2O
b. Na2S2O3与I2能发牛如下反应:I2+2Na2S2O3=2NaI+Na2S4O6
①配制100.00mL0.01500mol/LI2标准溶液,所必需的玻璃仪器有烧杯、玻璃棒、胶头滴管和____。
②向饮料中加入稀硫酸并充分煮沸的目的是___________。
③计算该饮料中糖类物质的含量(单位mg/mL)(写出计算过程)。______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某密闭恒容的容器内可逆反应A(g)+3B(g)![]() 2C(g)达到平衡状态的标志
2C(g)达到平衡状态的标志
A. A的消耗速率是C的分解速率1/2倍
B. 容器内混合气体的密度不随时间而变化
C. 单位时间内生成nmolA,同时生成3nmolB
D. A、B、C的分子数之比为1:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验.
实验I:反应产物的定性探究,按如图装置(固定装置已略去)进行实验

(1)A装置的试管中发生反应的化学方程式是_____________________;F装置的烧杯中发生反应的离子方程式是__________________________;B装置中的现象是_________。
(2)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是______________ 。
(3)实验结束时,撤去所有酒精灯之前必须完成的实验操作是_________________。
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子,需将溶液稀释,操作方法是________________________________。
实验Ⅱ:反应产物的定量探究
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,且黑色物质为Cu2S。产生Cu2S的反应为aCu+bH2SO4 ![]() cCu2S+dCuSO4+e H2O,则a:b=______________。
cCu2S+dCuSO4+e H2O,则a:b=______________。
(6)为测定硫酸铜的产率,将该反应所得溶液中和后配制成250.00mL溶液,取该溶液25.00mL加入足量KI溶液中振荡,生成的I2恰好与20.00mL 0.30molL﹣1的Na2S2O3溶液反应,若反应消耗铜的质量为6.4g,则硫酸铜的产率为_________________。(已知2Cu2++4I﹣=2CuI+I2, 2S2O32﹣+I2=S4O62﹣+2I﹣) 【注:硫酸铜的产率指的是硫酸铜的实际产量与理论产量的比值】
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表是元素周期表的一部分,参照元素在表中的位置,请用化学用语回答下列问题:

(1)这些元素中,化学性质最不活泼原子的原子结构示意图为______;气态氢化物中,最稳定的是______;最高价氧化物对应水化物中,酸性最强的是_______。
(2)①和④两种元素的原子按1:1组成的常见化合物的电子式为______。
(3)②、③的单质中更容易与①的单质反应的是________(用化学式表示)。
(4)④、⑦、⑧、⑨的简单离子半径由大到小的顺序为_____(用离子符号和“>”表示)。
(5)⑥和⑧的最高价氧化物对应水化物之间发生反应的离子方程式____________。
(6)⑤⑨三种元素的单质沸点由高到低的顺序是_____(用化学式和“>”表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pOH=-lgc(OH-)。常温下,某弱酸的钠盐(Na2XO3)溶液中微粒浓度的变化关系如下图所示。下列说法正确的是

A. 实线M表示pOH与lg 的变化关系
的变化关系
B. 在NaHXO3溶液中:![]() >1
>1
C. 向Na2XO3溶液中滴加稀盐酸至溶液显中性时:c(Na+)+2c(H+)=c(HXO3-)+2c(XO32-)+2c(OH-)
D. Na2XO3溶液加水稀释,![]() 先增大后不变
先增大后不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com