
【题目】海洋是一个巨大的宝藏,期待着人们的开发和利用,下列物质不经过化学变化就能从海水中获得的是
A. 单质溴 B. 单质镁 C. 烧碱 D. 食盐
科目:高中化学 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度,实验时将样品放置于D中。(可供选用的反应物只有CaCO3固体、6 mol/L盐酸、6 mol/L硫酸和蒸馏水)
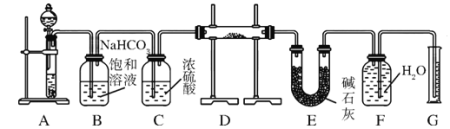
回答下列问题:
(1)装置A中液体试剂选用 。
(2)装置B的作用是 。装置C的作用是 。
装置E中碱石灰的作用是 。
(3)装置D中发生反应的化学方程式是 、 。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子或分子组中能大量共存,且满足相应要求的是
选项 | 离子或分子 | 要求 |
A | K+、NO | c(K+)<c(Cl-) |
B | Fe3+、NO | 滴加盐酸立即有气体产生 |
C | NH | 滴加NaOH溶液立即有气体产生 |
D | Na+、HCO | 滴加氨水立即有沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的气化可以减少环境污染,而且生成的CO和H2被称作合成气,能合成很多基础有机化工原料。
(1)工业上可利用CO生产乙醇:2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g) ΔH1
CH3CH2OH(g)+H2O(g) ΔH1
又知:H2O(l)=H2O(g) ΔH2
CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
工业上也可利用CO2(g)与H2(g)为原料合成乙醇:
2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(l) ΔH
CH3CH2OH(g)+3H2O(l) ΔH
则ΔH与ΔH1、ΔH2、ΔH3之间的关系是ΔH=____________。
(2)一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:4H2(g)+2CO(g)![]() CH3OCH3(g)+H2O(g),下列选项不能判断该反应达到平衡状态的是__________。
CH3OCH3(g)+H2O(g),下列选项不能判断该反应达到平衡状态的是__________。
A.v(H2)正=2v(CO)逆 B.平衡常数K不再随时间而变化
C.混合气体的密度保持不变 D.CH3OCH3和H2O的体积之比不随时间而变化
(3)工业可采用CO与H2反应合成再生能源甲醇,反应:CO(g)+2H2(g)![]() CH3OH(g),在一容积可变的密闭容器中充有10 mol CO和20 mol H2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(α)与温度(T)、压强(p)的关系如图1所示。
CH3OH(g),在一容积可变的密闭容器中充有10 mol CO和20 mol H2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(α)与温度(T)、压强(p)的关系如图1所示。

①合成甲醇的反应为______________(填“放热”或“吸热”)反应。
②A、B、C三点的平衡常数KA、KB、KC的大小关系为____________________。p1和p2的大小关系为___________。
③若达到平衡状态A时,容器的体积为10 L,则在平衡状态B时容器的体积为________L。
(4)工业上可通过甲醇羰基化法制取甲酸甲酯,其反应的热化学方程式为CH3OH(g)+CO(g)![]() HCOOCH3(g) ΔH2=-29.1 kJ·mol-1。科研人员对该反应进行了研究,部分研究结果如图2、3:
HCOOCH3(g) ΔH2=-29.1 kJ·mol-1。科研人员对该反应进行了研究,部分研究结果如图2、3:
①从反应压强对甲醇转化率的影响“效率”看,工业制取甲酸甲酯应选择的压强是________(填“3.5×106Pa”“4.0×106Pa”或“5.0×106Pa”)。
②实际工业生产中采用的温度是80℃,其理由是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对二氧化硫气体的物理性质或化学性质描述正确的有
A.无色、无味 B.容易液化、难溶于水
C.有漂白性,能使品红溶液褪色 D.和水反应生成硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是 ( )
A.Na2CO3是碱
B.Na2CO3是盐
C.Na2CO3是钠盐
D.Na2CO3是碳酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关二氧化碳的说法错误的是( )
A. 在空气中二氧化碳的体积分数约为0.03%
B. 二氧化碳有毒,不能供人呼吸
C. 过多的二氧化碳排放会导致温室效应
D. 干冰可用于人工降雨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢镍电池是近年开发出来的可充电电池,它可以取代会产生污染的铜镍电池。氢镍电池的总反应式是:
![]()
![]()
![]() 据此反应式判断,下列叙述中不正确的是
据此反应式判断,下列叙述中不正确的是
A. 电池放电时,电池负极周围溶液的PH不断增大
B. 电池放电时,正极的电极反应为:![]()
C. 电池充电时,阳极周围溶液的的PH不断减小
D. 电池充电时,阴极的电极反应为:2![]() +2
+2![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在pH=1的溶液中能大量共存的离子组合是( )
A.Ba2+、Na+、CO32﹣、SO42﹣
B.Mg2+、Cl﹣、Na+、SO42﹣
C.K+、Cl﹣、HCO3﹣、NO3﹣
D.K+、Na+、Fe2+、NO3﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com