
¹čĖįĶ±µŹĒµ±½ńÓĆ×īŠĀæĘѧ¼¼Źõ²ÅÄÜŗĻ³ÉµÄŅ»ÖÖĪļÖŹ”£Č»¶ųĻÖŌŚ·¢ĻÖ£¬ĪŅ¹śĒŲ³Æ±ųĀķŁøÓƵÄŅ»ÖÖŃÕĮĻ¾¹ŹĒ¹čĖįĶ±µ”£ĻĀĮŠ¹ŲÓŚ¹čĖįĶ±µµÄѧĖµ“ķĪóµÄŹĒ
A£®Ņ×ČÜÓŚĖ® B£®ÄŃČÜÓŚĖ® C£®ŹōÓŚ¹čĖįŃĪ D£®ÓŠŃÕÉ«
 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijĢžÓėĒāĘų¼Ó³ÉŗóµĆµ½2,2¶ž¼×»ł¶”Ķ飬øĆĢžµÄĆū³ĘæÉÄÜŹĒ
(””””)
A£®3,3¶ž¼×»ł1¶”Č² B£®2,2¶ž¼×»ł2¶”Ļ©
C£®2,2¶ž¼×»ł1¶”Ļ© D£®3,3¶ž¼×»ł1¶”Ļ©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆCH4“߻ƻ¹ŌNOx£¬æÉŅŌĻū³żµŖŃõ»ÆĪļµÄĪŪČ¾”£ĄżČē£ŗ
¢ŁCH4(g)£«4NO2(g)===4NO(g)£«CO2(g)£«2H2O(g) ¦¤H£½£574 kJ·mol£1
¢ŚCH4(g)£«4NO(g)===2N2(g)£«CO2(g)£«2H2O(g) ¦¤H£½£1 160 kJ·mol£1
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
A£®ČōÓƱź×¼×“æöĻĀ4.48 L CH4»¹ŌNO2Éś³ÉN2ŗĶĖ®ÕōĘų£¬·Å³öµÄČČĮæĪŖ173.4 kJ
B£®ÓÉ·“Ó¦¢ŁæÉĶĘÖŖ£ŗCH4(g)£«4NO2(g)===4NO(g)£«CO2(g)£«2H2O(l)””¦¤H<£574 kJ·mol£1
C£®·“Ó¦¢Ł¢Ś×ŖŅʵĵē×ÓŹżĻąĶ¬
D£®·“Ó¦¢ŚÖŠµ±4.48 L CH4·“Ó¦ĶźČ«Ź±×ŖŅʵĵē×Ó×ÜŹżĪŖ1.60 mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚ11Na”¢12Mg”¢13Al”¢14Si”¢15P”¢16S”¢17Cl”¢18Ar°ĖÖÖŌŖĖŲÖŠ£¬ÄÜ
ÓƱķŹ¾ŗĖĶāµē ×ÓÅŲ¼µÄ³£¼ūŃōĄė×Ó¹²ÓŠ
A£®1ÖÖ B£®2ÖÖ C£®3ÖÖ D£®4ÖÖ

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠø÷×éČÜŅŗÖŠ£¬Ąė×ÓŅ»¶ØÄÜ“óĮæ¹²“ęµÄŹĒ
A£®ĒæĖįČÜŅŗÖŠ£ŗNa+”¢Mg2+”¢SO42-”¢AlO2-
B£®Ä³ĪŽÉ«ČÜŅŗÖŠ£ŗNH4+”¢Cu2+”¢MnO4-”¢NO3-
C£®ŗ¬ÓŠ0.1 mol/L Fe3+ČÜŅŗÖŠ£ŗK+”¢Mg2+”¢Cl-”¢SCN-
D£®ÓėĀĮ·“Ӧɜ³ÉH2µÄČÜŅŗÖŠ£ŗNa+”¢K+”¢Cl-”¢SO42-
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻņŅ»¶ØĮæFe”¢FeO”¢Fe2O3µÄ»ģŗĻĪļÖŠ£¬¼ÓČė50mL 1mol/LĮņĖį£¬Ē”ŗĆŹ¹»ģŗĻĪļĶźČ«Čܽā£¬·Å³ö224mL£Ø±ź×¼×“æö£©µÄĘųĢ壬ĖłµĆČÜŅŗÖŠ¼ÓČėKSCNČÜŅŗĪŽŃŖŗģÉ«³öĻÖ”£ČōÓĆ×ćĮæµÄCOŌŚøßĪĀĻĀ»¹ŌĻąĶ¬ÖŹĮæµÄ»ģŗĻĪļ£¬ÄܵƵ½ĢśµÄÖŹĮæĪŖ
A£®11.2g B£®5.6g C£®2.8g D£®ĪŽ·Ø¼ĘĖć
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¹ŲÓŚĪļÖŹµÄ·ÖĄąÕżČ·µÄŹĒ£Ø £©
A£®SO2”¢CO2”¢CO”¢NO2¶¼ŹĒĖįŠŌŃõ»ÆĪļ
B£®Na2O”¢Na2O2”¢Fe2O3”¢CuO¶¼ŹĒ¼īŠŌŃõ»ÆĪļ
C£®HCl”¢HClO”¢HNO3”¢HClO4¶¼ŹĒĒæĖį
D£®NaOH”¢KOH”¢Ba(OH)2”¢Ca(OH)2¶¼ŹĒĒæ¼ī
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠµÄĄė×Ó·½³ĢŹ½ÖŠ£¬ŹéŠ“ÕżČ·µÄŅ»ĻīŹĒ£Ø £©
A£®°±Ė®ÖŠĶØČė¹żĮæCO2£ŗ2NH3”¤H2O +CO2==== 2NH4++CO32-+H2O
B£®Ļ”ĻõĖįÖŠ¼ÓČė¹żĮæĢś·Ū£ŗ3Fe + 8H£«+2 NO3£==== 3Fe2£«+ 2NO”ü + 4H2O
C£®ÄĘÓėĖ®·“Ó¦ Na+2H2O==== Na+ +2OH£+H2 ”ü
D£®Ca(ClO)2 ČÜŅŗÖŠĶØČė¹żĮæµÄ¶žŃõ»ÆĮņĘųĢå£ŗClO-+SO2+H2O==== HClO+HSO3-
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
(1)ŌŚ25”ꏱ£¬ĻņÅØ¶Č¾łĪŖ0.01 mol”¤L£1µÄMgCl2ŗĶAlCl3»ģŗĻČÜŅŗÖŠÖšµĪ¼ÓČė°±Ė®£¬ĻČÉś³É________³Įµķ(Ģī»ÆѧŹ½)£¬Éś³ÉøĆ³ĮµķµÄĄė×Ó ·½³ĢŹ½ĪŖ_____________________”£
·½³ĢŹ½ĪŖ_____________________”£
(ŅŃÖŖ25”ꏱKsp[Mg(OH)2]£½1.8”Į10£11£¬
Ksp[Al(OH)3]£½3”Į10£34”£)
(2)ijĪĀ¶Č(t”ę)Ź±£¬²āµĆ0.01 mol”¤L£1µÄNaOHČÜŅŗµÄpH£½11”£ŌŚ“ĖĪĀ¶ČĻĀ£¬½«pH£½2µÄH2SO4ČÜŅŗVaLÓėpH£½12µÄNaOHČÜŅŗVbL»ģŗĻ£¬ČōĖłµĆ»ģŗĻŅŗĪŖÖŠŠŌ£¬ŌņVa©UVb£½________”£
(3)ŌŚ25”ꏱ£¬½«c mol”¤L£1µÄ“×ĖįČÜŅŗÓė0.02 mol”¤L£1NaOHČÜŅŗµČĢå»ż»ģŗĻŗóČÜŅŗøÕŗĆ³ŹÖŠŠŌ£¬ÓĆŗ¬cµÄ“śŹżŹ½±ķŹ¾CH3COOHµÄµēĄė³£ŹżKa£½________”£
(4)(2013”¤É½¶«øßæ¼)25”ꏱ£¬H2SO3HSO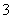 £«H£«µÄµēĄė³£ŹżKa£½1”Į10£2mol”¤L£1£¬ŌņøĆĪĀ¶ČĻĀNaHSO3Ė®½ā·“Ó¦µÄĘ½ŗā³£ŹżKb£½________mol”¤L£1£¬ČōĻņNaHSO3ČÜŅŗÖŠ¼ÓČėÉŁĮæµÄI2£¬ŌņČÜŅŗÖŠ
£«H£«µÄµēĄė³£ŹżKa£½1”Į10£2mol”¤L£1£¬ŌņøĆĪĀ¶ČĻĀNaHSO3Ė®½ā·“Ó¦µÄĘ½ŗā³£ŹżKb£½________mol”¤L£1£¬ČōĻņNaHSO3ČÜŅŗÖŠ¼ÓČėÉŁĮæµÄI2£¬ŌņČÜŅŗÖŠ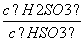 ½«________(Ģī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±)”£
½«________(Ģī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±)”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com