
 �ұ��������Ʊ���ϩ��Ӧ��ͼ1��
�ұ��������Ʊ���ϩ��Ӧ��ͼ1��| ��ѧ�� | C-H | C-C | C�TC | H-H |
| ����/kJ•mol-1 | X | 348 | 612 | 436 |
���� ��1����Ӧ��=��Ӧ���ܼ���-���������ܼ��ܣ����л���Ľṹ��֪��Ӧ��-CH2CH3���ܼ�����-CH=CH2��H2�ܼ���֮�
��2���μӷ�Ӧ���ұ�Ϊn�� mol����
 ?
? +H2
+H2
��ʼ��mol����n 0 0
ת����mol����n�� n�� n��
ƽ�⣨mol����n��1-���� n�� n��
ά����ϵ��ѹǿp�㶨������ƽ��ʱ����ַ�ѹ���ٸ���Kp=$\frac{p�������ᣩP��H{\;}_{2}��}{P���ұ���}$���㣬���ڸ���ϵ�Ǻ�ѹ��ϵ��������ƽ����ϵ�г�������������������ڷ�Ӧ��ϵ�൱�ڼ�ѹ��
��3���ٱ���ѹǿ���䣬����ˮ�������������Ӧ����ЧΪ����ѹǿ��ƽ���������������ķ����ƶ���
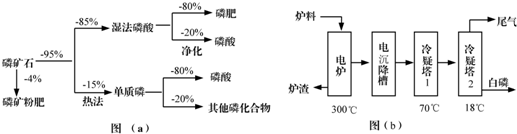
��600��ʱ�ұ���ת�����뱽��ϩ��ѡ���Ծ��ϸߣ�����¶ȶ��ұ�ת���ʡ�����ϩѡ���ԡ��¶ȶԷ�Ӧ�����������Ӱ�켰���������ȣ��������Ʒ�Ӧ�¶�Ϊ600������ɣ�
��4����CO2��H2��Ӧ����������Ũ�ȼ��ͣ��������ұ����ⷴӦ�Ļ�ѧƽ�����ƣ�
������Ŀ��Ϣ��֪���ڱ��ֳ�ѹ��ԭ�����������䣬���ˮ����������ȣ�����ͬ������Ч���£��ɽ��Ͳ����¶ȣ����ĵ��������٣�
�����ڻᷢ����ӦCO2+C�T2CO�������ڼ��ٻ�̿��
��CO2����ˮ������������CO2��Դ���ã�
��5���������⣬��������һ������Ϊ������������ȼ�ϵ�صIJ��ϣ������ڸ�������������Ӧ���������Ϊ����̼���Σ�����̼����������ɶ�����̼��ˮ��
��� �⣺��1����Ӧ��=��Ӧ���ܼ���-���������ܼ��ܣ����л���Ľṹ��֪��Ӧ��-CH2CH3���ܼ�����-CH=CH2��H2�ܼ���֮��ʡ�H=��5��X+348-3��X-612-436��kJ•mol-1=+124kJ•mol-1������X=412��
�ʴ�Ϊ��412��
��2�����ʵ���Ϊn���ұ��������������ⷴӦ���μӷ�Ӧ���ұ�Ϊn�� mol����
 ?
? +H2
+H2
��ʼ��mol����n 0 0
ת����mol����n�� n�� n��
ƽ�⣨mol����n��1-���� n�� n��
ά����ϵ��ѹǿp�㶨��ѹǿƽ�ⳣ��Kp=$\frac{p�������ᣩP��H{\;}_{2}��}{P���ұ���}$=$\frac{\frac{n��}{n��1+����}p��\frac{n��}{n��1+����}p}{\frac{n��1-����}{n��1+����}p}$=$\frac{��{\;}^{2}}{��1-��{\;}^{2}��}p$�����ڸ���ϵ�Ǻ�ѹ��ϵ��������ƽ����ϵ�г�������������������ڷ�Ӧ��ϵ�൱�ڼ�ѹ�����Է�Ӧ���ʻ��С��
�ʴ�Ϊ��$\frac{��{\;}^{2}}{��1-��{\;}^{2}��}p$����С��
��3��������ӦΪ�������������ķ�Ӧ������ѹǿ���䣬����ˮ�������������Ӧ����ЧΪ����ѹǿ��ƽ��������Ӧ�����ƶ�������ұ���ƽ��ת���ʣ�
�ʴ�Ϊ������ӦΪ�������������ķ�Ӧ������ѹǿ���䣬����ˮ�������������Ӧ����ЧΪ����ѹǿ��ƽ��������Ӧ�����ƶ���
��600��ʱ�ұ���ת�����뱽��ϩ��ѡ���Ծ��ϸߣ��¶ȹ��ͣ���Ӧ���ʽ�����ת���ʽϵͣ��¶ȹ��ߣ�ѡ�����½��������¿���ʧ����ʧȥ���ԣ������������ϴ�ѡ��600�����ң�
�ʴ�Ϊ��600��ʱ�ұ���ת�����뱽��ϩ��ѡ���Ծ��ϸߣ��¶ȹ��ͣ���Ӧ���ʽ�����ת���ʽϵͣ��¶ȹ��ߣ�ѡ�����½��������¿���ʧ����ʧȥ���ԣ������������ϴ�
��4����CO2��H2��Ӧ����������Ũ�ȼ��ͣ��������ұ����ⷴӦ�Ļ�ѧƽ�����ƣ�����ȷ��
������Ŀ��Ϣ��֪���ڱ��ֳ�ѹ��ԭ�����������䣬���ˮ����������ȣ�����ͬ������Ч���£��ɽ��Ͳ����¶ȣ����ĵ��������٣�����ȷ��
�����ڻᷢ����ӦCO2+C�T2CO�������ڼ��ٻ�̿������ȷ��
��CO2����ˮ������������CO2��Դ���ã�����ȷ��
�ʴ�Ϊ���٢ڢۢܣ�
��5���������⣬��������һ������Ϊ������������ȼ�ϵ�صIJ��ϣ��������Ϊ����̼���Σ��为���缫��ӦʽΪH2-2e-+CO32-=H2O+CO2����
�ʴ�Ϊ��H2-2e-+CO32-=H2O+CO2����
���� ���⿼�鷴Ӧ�ȼ��㡢��ѧƽ�ⳣ�����㡢��Ӧ���ʼ�ƽ���ƶ���Ӱ�����ء����������Ƶķ������۵ȣ���1������Ϊ�������ڵ�˫��������ʽ��Ӱ�����ṹ����Ŀ�ѶȽϴ�


 ʱ�����������ҵԭ���ܳ�����ϵ�д�
ʱ�����������ҵԭ���ܳ�����ϵ�д� ����νӽ̲���ĩ���Ԥϰ�人������ϵ�д�
����νӽ̲���ĩ���Ԥϰ�人������ϵ�д� ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2O2��������������Na2O���� | |
| B�� | ���ڳ����²����ױ����� | |
| C�� | Na2O��Na2O2���ܺ�ˮ��Ӧ���ɼ���Ƕ��Ǽ��������� | |
| D�� | ����������ȼ�գ����ɰ�ɫ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 A��B��C��D���ֶ�����Ԫ�أ���A��B��DΪ���ڵ�ͬ����Ԫ�أ�C��Bͬ���壬B��C���γɹ��ۻ�����BC3��BC2��A��ԭ�ӽṹʾ��ͼͼ���ݴ���գ�
A��B��C��D���ֶ�����Ԫ�أ���A��B��DΪ���ڵ�ͬ����Ԫ�أ�C��Bͬ���壬B��C���γɹ��ۻ�����BC3��BC2��A��ԭ�ӽṹʾ��ͼͼ���ݴ���գ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| �۵�/�� | �е�/�� | ��ע | |
| ���� | 44 | 280.5 | |
| PH3 | -133.8 | -87.8 | ������ˮ���л�ԭ�� |
| SiF4 | -90 | -86 | ��ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��C2B2������ѧ��Ϊ���Ӽ������ۼ���
��C2B2������ѧ��Ϊ���Ӽ������ۼ���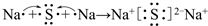 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ������0.1 mol•L-1 NaOH��Һ��Ӧ��H+��aq��+OH-��aq���TH2O��l����H=-57.3 kJ•mol-1 | |
| B�� | �����ı�ȼ����Ϊ285.5 kJ•mol-1����ˮ�ֽ���Ȼ�ѧ����ʽ��2H2O��l���T2H2��g��+O2��g����H=285.5 kJ•mol-1 | |
| C�� | �ܱ������У�9.6 g�����11.2 g���ۻ�ϼ�������������17.6 gʱ���ų�19.12 kJ������ ��Fe��s��+S��s���TFeS��s����H=-95.6 kJ•mol-1 | |
| D�� | ��֪2C��s��+O2��g���T2CO��g����H=-221 kJ•mol-1�����֪C�ı�ȼ����Ϊ110.5 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SiO2������HF��Ӧ��������NaOH��Ӧ����������������� | |
| B�� | SO2��Cl2����Ư�����ʣ������ߵ����ʵ�����ϣ�Ư��Ч�����ǿ | |
| C�� | ������NaͶ��FeCl3��Һ�У��ɽ�Fe3+ֱ�ӻ�ԭΪFe���� | |
| D�� | 1 mol Na2O2��������CO2��Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ1 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C2H4 | B�� | C4H6 | C�� | C3H8 | D�� | C6H6 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com