
【题目】只用一种试剂或操作,除去下列物质中的杂质(括号内为杂质)写出试剂或操作的名称、方法及有关的化学方程式或离子方程式:
(1)Fe2O3(Al2O3)_________________;离子方程式__________。
(2)Fe2O3[Fe(OH)3]________;化学方程式_______________。
(3)FeSO4溶液(CuSO4)_____________;离子方程式_________。
(4)FeCl3溶液(FeCl2)_____________;离子方程式__________。
【答案】加足量氢氧化钠溶液溶解,然后过滤 Al2O3+2OH-![]() 2AlO2-+H2O加热2Fe(OH)3
2AlO2-+H2O加热2Fe(OH)3![]() Fe2O3+3H2O加足量铁粉,充分反应后过滤Cu2++Fe
Fe2O3+3H2O加足量铁粉,充分反应后过滤Cu2++Fe![]() Fe2++Cu通入适量氯气2Fe2++Cl2
Fe2++Cu通入适量氯气2Fe2++Cl2![]() 2Fe3++2Cl-
2Fe3++2Cl-
【解析】
(1)氧化铝是两性氧化物,能和氢氧化钠反应,而氧化铁则不能,可加入足量的氢氧化钠溶液除去氧化铝,再过滤分离即可,离子方程式为:Al2O3+2OH-═2AlO2-+H2O;
(2)Fe(OH)3加热分解生成氧化铁,故选择方法为加热,化学方程式为:2Fe(OH)3![]() Fe2O3+3H2O;
Fe2O3+3H2O;
(3)加入足量的铁粉,铁与硫酸铜反应生成硫酸亚铁和铜,然后过滤,滤液即为硫酸亚铁,离子方程式为:Fe+Cu2+=Cu+Fe2+;
(4)通入足量的氯气,氯气与氯化亚铁溶液反应生成氯化铁,离子方程式为:Cl2+2Fe2+=2Cl-+2Fe3+。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质。下列说法错误的是( )

A. 溶液中K+向电极b移动
B. 氨气在电极a上发生氧化反应
C. 反应消耗的NH3与O2的物质的量之比为4:3
D. 正极的电极反应式为:O2+4e-+2H2O=4OH-,故反应一段时间后,电解液的pH升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某饱和溶液中含有三种阳离子:Ag+、Ba2+、Al3+,同时测知此溶液中pH=3,则该溶液中所含有的阴离子可以是下列中的()
A.CO32-B.SO42-C.NO3-D.Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种化合物,均含有某种常见元素,它们的转化关系如下图所示,其中A为澄清溶液,C为难溶于水的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。请回答下列问题:

(1)写出化学式:A__________C__________
(2)写出下列反应的离子方程式:
A→B:________________________________。
B→D:________________________________。
C→E:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)Na2CO3固体中混有少量NaHCO3固体,除去杂质的方法是________________,化学方程式是___________________________________。
(2)NaHCO3固体中混有少量Na2CO3固体,除杂方法是________________,化学方程式是________________________________________________________。
(3)NaOH固体中混有少量Na2CO3固体,除杂方法是________________,反应的离子方程式是_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用含少量银和锌的粗铜做阳极,纯铜片做阴极,CuSO4溶液做电解液,电解一段时间后,阳极质量减少了x g,则( )
A. 电解液质量增加x g B. 阴极质量增加x g
C. 阴极质量增加a g,a>x D. 阴极质量增加b g,b<x
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH=-a kJ·mol-1 在5 L密闭容器中进行,10 s时,水蒸气的物质的量增加了0.60 mol。则下列说法不正确的是( )
4NO(g)+6H2O(g) ΔH=-a kJ·mol-1 在5 L密闭容器中进行,10 s时,水蒸气的物质的量增加了0.60 mol。则下列说法不正确的是( )
A. 10 s内,NH3的平均反应速率为0.008 mol·L-1·s-1
B. 该反应达到平衡时6v正(O2)=5v逆(H2O)
C. 10 s内,反应放出的热量为0.1a kJ
D. 10 s时,H2O的反应速率为0.012 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请用下图所示仪器装置设计一个包括电解饱和食盐水并测定电解时产生的氢气的体积和检验氯气的氧化性的实验装置。
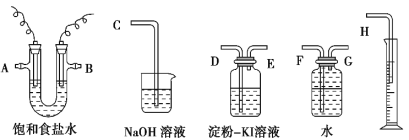
(1)所选仪器 连接时,各接口的顺序是(填各接口的代号字母):A 接 , 接 ,B 接 , 接 。_____________
(2)实 验 时 , 装 置 中 的 石 墨 电 极 接 电 源 的 _____极 , 所 发 生 的 电 极 反 应 式 为_____;铁电极接电源的_____极,所发生的电极反应式为_____; 此电解总反应方程式为_________。
(3)实验测得产生的氢气体积(已折算成标准状况)为 5.60 mL,电解后溶液的体积恰好为50.0 mL,则溶液中 OH-的浓度为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰基烯酸酯在碱性条件下能快速聚合为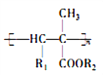 ,从而具有胶黏性,某种氰基丙烯酸酯(H)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(H)的合成路线如下:
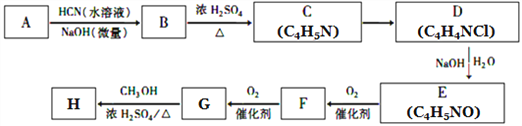
已知:①A的相对分子量为58,氧元素质量分数为0. 276,核磁共振氢谱显示为单峰;
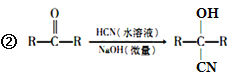
回答下列问题:
(1)A的化学名称为____________。
(2)C的结构简式为________________,F中的含氧官能团名称是________________。
(3)由E生成F的反应类型为_____________,由G生成H的反应类型为_____________。
(4)由G生成H的化学方程式为________________________________。
(5)写出A的能够发生银镜反应的同分异构体的结构简式______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com