
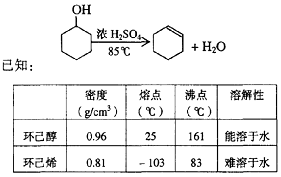
某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇为主要原料制备环己烯。
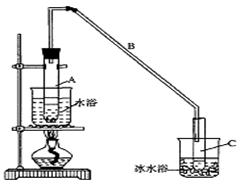
(1)制备粗品
将12.5 mL环己醇加入试管A中,再加入l mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是____________,导管B除了导气外还具有的作用是____________。
②试管C置于冰水浴中的目的是______________________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_________层(填上或下),分液后用_________ (填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
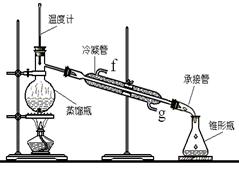
②再将环己烯按下图装置蒸馏,冷却水从_________口进入(填“g”或“f”)。收集产品时,控制的温度应在_________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是________________________
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
下列离子方程式书写正确的是
A.在NaClO溶液中通入过量SO2气体:ClO-+H2O+SO2=HClO+HSO3-
B.用稀氢碘酸溶液除去铁制品表面的铁锈:Fe2O3+6H+ =2Fe3+ +3H2O
C.NaHCO3与少量的Ca(OH)2溶液反应:Ca2++2OH-+2HCO3- = CaCO3↓+2H2O+CO32-
D.10mL0.5mol/L的明矾溶液与20mL0.5mol/LBa(OH)2溶液混合反应:3Ba2+ + 6OH- +2Al3+ +3SO42- = 3BaSO4↓+2Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
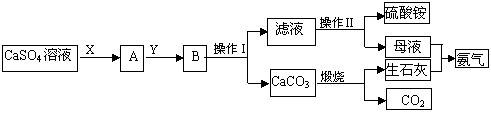
某化学小组在实验中利用CaSO4、NH3、CO2制备(NH4)2SO4,其工艺流程如下。
回答下列问题:
(1)操作Ⅰ的名称为_________;操作Ⅱ一系列操作包括蒸发浓缩、________、过滤。
(2)实验室中煅烧碳酸钙时,盛放碳酸钙所用的仪器是________(填名称)。
(3)X物质为____(填化学式,下同),Y物质为____,可循环利用的物质的有_____。
(4)要测定所制得的硫酸铵纯度,取10.0g样品,完全溶于水,向溶液中滴加过量的氯化钡溶液,过滤、洗涤、干燥后称量固体的质量为16.31g。为避免引起误差,检验氯化钡溶液是否过量最好的试剂是_______,所制得硫酸铵的纯度为________。
(5)下列装置不能用于实验室制氨气的是__________(填序号)。

选择氨气的制取装置后,再用下列装置收集干燥的氨气,并制取硫酸铵溶液,连接的顺序(用接口序号字母表示)是:a接____,____接____,____接_____,____接_____。
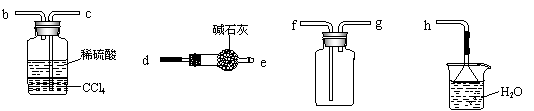
上述装置中CCl4的作用是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
蔗糖酯是联合国国际粮农组织和世界卫生组织推荐使用的食品乳化剂。某蔗糖酯可由蔗糖与硬脂酸乙酯合成,反应如下:

蔗糖 蔗糖酯
有关说法不正确的是( )
A.蔗糖酯可看成是由高级脂肪酸和蔗糖形成的酯
B.合成该蔗糖酯的反应属于取代反应
C.蔗糖不能发生银镜反应,而它的同分异构体纤维二糖则能发生银镜反应。
D.该蔗糖酯在稀硫酸作用下水解,水解后只有硬脂酸和葡萄糖两种产物
查看答案和解析>>
科目:高中化学 来源: 题型:
食品香精菠萝酯的生产路线(反应条件略去)如下:
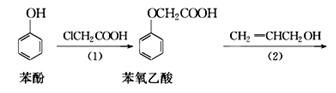

下列叙述错误的是( )
A.步骤(1)产物中残留的苯酚可用FeCl3溶液检验
B.苯酚和菠萝酯均可与酸性KMnO4溶液发生反应
C.苯氧乙酸和菠萝酯均可与NaOH溶液发生反应
D.步骤(2)产物中残留的烯丙醇可用溴水检验
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.构成单质分子的微粒一定含有共价键
B.熔融时能导电的化合物,一定是离子化合物
C.水加热至1000℃也不分解,是由于水分子间存在氢键
D.由H原子形成1 mol H-H键所要吸收的能量就等于H-H的键能
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省淄博市高二12月月考化学试卷(解析版) 题型:选择题
在甲酸的下列性质中,可以证明它是弱电解质的是
A.1mol/L的甲酸溶液中c(H+)约为1×10-2 mol/L
B.甲酸能与水以任意比例互溶
C.1mol/L的甲酸溶液10mL恰好与10mL1mol/L的NaOH溶液完全反应
D.甲酸溶液的导电性比盐酸弱
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邢台市高二12月月考化学试卷(解析版) 题型:填空题
(11分)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下列各题:
元素代号 | I1 | I2 | I3 | I4 |
Q | 2 080 | 4 000 | 6 100 | 9 400 |
R | 500 | 4 600 | 6 900 | 9 500 |
S | 740 | 1 500 | 7 700 | 10 500 |
T | 580 | 1 800 | 2 700 | 11 600 |
U | 420 | 3 100 | 4 400 | 5 900 |
(1)在周期表中,最可能处于同一族的是________。
A.Q和R
B.S和T
C.T和U
D.R和T
E.R和U
(2)下列离子的氧化性最弱的是________。
A.S2+ B.R2+ C.T3+ D.U+
(3)下列元素中,化学性质和物理性质最像Q元素的是______________________________。
A.硼 B.铍 C.氦 D.氢
(4)每种元素都出现相邻两个电离能的数据相差较大的情况,这一事实从一个侧面说明:________________________________________________________________________,
如果U元素是短周期元素,你估计它的第2次电离能飞跃数据将发生在失去第____个电子时。
(5)如果R、S、T是同周期的三种主族元素,则它们的原子序数由小到大的顺序是__________,其中________元素的第一电离能异常高的原因是_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com