
下列叙述正确的是()
A. 氧气的摩尔质量为32g B. 1molH2SO4的质量98
C. H2O的摩尔质量18g•mol﹣1 D. 1molCH4体积为22.4L
考点: 摩尔质量.
专题: 阿伏加德罗常数和阿伏加德罗定律.
分析: A、摩尔质量的单位是g/mol;
B、质量的单位是g;
C、摩尔质量的单位是g/mol,数值上等于其相对分子质量;
D、标况下,1mol任何气体的体积是22.4L.
解答: 解:A、摩尔质量的单位是g/mol,故氧气的摩尔质量为32g/mol,故A错误;
B、质量的单位是g,故1molH2SO4的质量是98g,故B错误;
C、摩尔质量的单位是g/mol,数值上等于其相对分子质量,故C正确;
D、标况下,1mol任何气体的体积是22.4L,未说明气体的状态,故D错误,故选C.
点评: 本题主要考查的是摩尔质量的定义以及单位,摩尔质量的单位是g/mol,注意与质量的区别.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
以下有关原子结构及元素周期律的叙述正确的是( )
A.第ⅠA族元素铯的两种同位素137Cs比133Cs多4个质子
B.同周期元素(除0族元素外)从左到右,原子半径逐渐减小
C.第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强
D.同主族元素从上到下,单质的熔点逐渐降低
查看答案和解析>>
科目:高中化学 来源: 题型:
所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细。由此判断表中所列M、N、P物质,其中可以成立的是( )
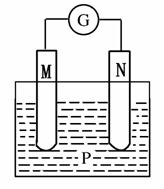
| 选项 | M | N | P |
| A | Zn | Cu | 稀H2SO4溶液 |
| B | Cu | Fe | 稀HCl溶液 |
| C | Ag | Zn | AgNO3溶液 |
| D | Zn | Fe | FeSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学在用稀硫酸与锌反应制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有__________________。
(2)硫酸铜溶液可以加快氢气生成速率的原因是____________。
(3)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是________。
(4)要加快上述实验中气体产生的速率,还可采取的措施有________________________________________________________(答两种)。
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
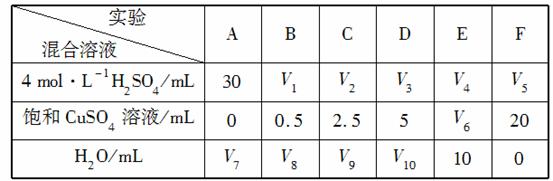
①请完成此实验设计,其中:V1=________,V6=________,V9=________;
②反应一段时间后,实验A中的金属呈________色,实验E中的金属呈________色;
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:
___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. 18gH2O含10NA个电子
B. 标况下1molH2O体积22.4L
C. 11.2LCH4物质的量一定为0.5mol
D. 标况下22.4LH2含NA个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学按图所示的装置进行电解实验.下列说法正确的是()
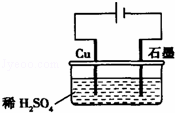
A. 电解过程中,铜电极上有H2产生
B. 电解初期,主要反应方程式为:Cu+H2SO4 CuSO4+H2↑
CuSO4+H2↑
C. 电解一定时间后,石墨电极上有铜析出
D. 整个电解过程中,H+的浓度不断增大
查看答案和解析>>
科目:高中化学 来源: 题型:
白磷与氧气可发生如下反应:P4+5O2===P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ·mol-1、P—O b kJ·mol-1、P===O c kJ·mol-1、O===O d kJ·mol-1。
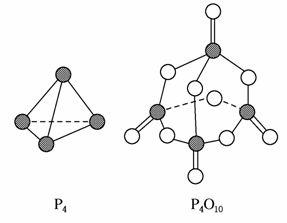
根据图示的分子结构和有关数据估算该反应的ΔH,其中正确的是( )
A.(6a+5d-4c-12b)kJ·mol-1
B.(4c+12d-6a-5d)kJ·mol-1
C.(4c+12b-4a-5d)kJ·mol-1
D.(4a+5d-4c-12b)kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com