
分析 沉淀干燥后质量8.0g为碳酸钙质量,据此求出二氧化碳的物质的量,根据二氧化碳的物质的量计算出铅氧化物中氧原子的物质的量及氧元素的质量,再计算出铅元素的质量即铅原子的物质的量,据此书写化学式.
解答 解:沉淀干燥后质量8.0g为碳酸钙质量,
所以碳酸钙的物质的量为$\frac{8.0g}{100g/mol}$=0.08mol,铅氧化物中的氧原子被CO夺取生成CO2,
根据碳元素、氧元素守恒可知CO~~~O~~~CO2~~~CaCO3,
1 1 1
0.08mol 0.08mol 0.08mol
所以铅氧化物中的氧原子的物质的量为0.08mol,氧元素的质量为0.08mol×16g/mol=1.28g;
所以铅氧化物中的铅元素的质量为13.7g-1.28g=12.42g,铅原子的物质的量为$\frac{12.42g}{207g/mol}$=0.06mol,
所以铅氧化物中铅原子与氧原子的物质的量之比为0.06mol:0.08mol=3:4,所以铅氧化物的化学式为Pb3O4,答:铅氧化物的化学式为Pb3O4.
点评 本题考查学生利用化学反应球物质的化学式,明确反应中元素的守恒来分析铅氧化物中氧元素的质量是解答的关键.


科目:高中化学 来源: 题型:选择题
| A. | Cl2 | B. | Fe3+ | C. | HNO3 | D. | MnO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
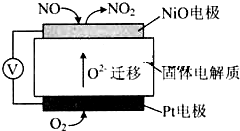 某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5um的悬浮颗粒物)其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5um的悬浮颗粒物)其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol.L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体中一定有NO2和CO | B. | 混合气体中一定没有H2和NH3 | ||
| C. | 不能确定混合气体中是否有NH3 | D. | 混合气体中至少有HCl等四种气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
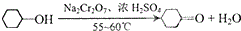 实验室用Na2Cr2O7氧化环己醇制取环己酮(已知该反应为放热反应):
实验室用Na2Cr2O7氧化环己醇制取环己酮(已知该反应为放热反应):| 物质 | 沸点( ) | 密度(g.cm-3,20) | 溶解性 |
| 环己醇 | 161.1(97.8) | 0.9624 | 能溶于水和乙醚 |
| 环己酮 | 155.6(95) | 0.9478 | 微溶于水,能溶于乙醚 |
| 水 | 100.0 | 0.9982 |
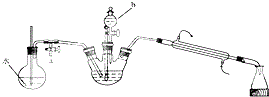
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入5.6g 铁粉充分反应后,溶液红色褪去 | |
| B. | 加入40mL水充分振荡后,静置,溶液红色变浅 | |
| C. | 加入10g Fe2(SO4)3固体充分反应后,溶液红色明显加深 | |
| D. | 加入20mL 0.001 mol/L KSCN溶液充分反应后,溶液红色明显变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
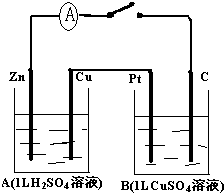
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com