
为探索工业含铝、铁、铜合金废料的再利用,甲同学设计的实验方案如下:
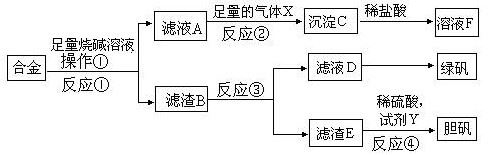
请回答:
(1)绿矾的化学式为 。
(2)写出反应①的 化学方程式 ,
化学方程式 ,
反应②生成沉淀的离子反应方程式 。
(3)为了检测滤液D中含有的金属离子,可设计实验方案为(试剂自选): 。
(4)在滤渣B中滴加稀硫酸时,发现反应速率比一般的铁粉反应要快,其原因是 。
(5)若考虑绿色化学工艺,在滤渣E中加入稀硫酸和试剂Y制胆矾晶体,试剂Y为无色液体,则反应④的总化学方程式为 ;若不考虑绿色化学工艺,所选试剂Y为1mol/L的硝酸,欲使3molCu全部溶解且溶液中含铜元素的溶质仅为CuSO4,则需该硝酸的体积 L。
碱石灰
(1)FeSO4·7H2O
(2) 2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2 ↑ ,
CO2 + 2H2O + AlO2- =Al(OH)3+ HCO3-
(3)用试管取少量滤液D,向滤液中滴加KSCN溶液无明显现象,再滴入氯水,若变成血红色,则说明溶液中存在Fe2+。
(4)铜、铁与稀硫酸形成原电池
(5)Cu + H2O2 +H2SO4 = CuSO4 + 2H2O ; 2
【解析】(1)绿矾为硫酸亚铁晶体,化学式为:FeSO4·7H2O
(2)反应①为Al与NaOH溶液的反应,离子方程式为:
2Al+2NaOH+2H2O 2NaAlO2+3H2↑;
2NaAlO2+3H2↑; 反应②中通入的气体气体X为CO2,CO2、H2O与AlO2-反应生成的沉淀为Al(OH)3,离子方程式为:
反应②中通入的气体气体X为CO2,CO2、H2O与AlO2-反应生成的沉淀为Al(OH)3,离子方程式为:
AlO2-+CO2+2H2O Al(OH)3↓+HCO3-(或2AlO2-+CO2+3H2O
Al(OH)3↓+HCO3-(或2AlO2-+CO2+3H2O 2Al(OH)3↓+CO32-)
2Al(OH)3↓+CO32-)
(3)滤液D的溶质为FeSO4,检验Fe2+的原理为:Fe2+不能使KSCN变为血红色,但加入氧化剂把Fe2+氧化为Fe3+,溶液变为血红色,所以实验方案为:用试管取少量滤液D,向滤液中滴加KSCN(或NaSCN、或NH4SCN)],溶液无明显现象,再滴入氯水(或双氧水,或通入Cl2)若变成血红色,则溶液则中存在Fe2+。
(4)滤渣B中含有铁、铜金属,滴加稀硫酸后,铜、铁与稀硫酸形成了原电池,使反应速率加快。
(5)滤渣E为Cu,加入稀硫酸和试剂Y生成CuSO4,考虑绿色化学工艺,Y为无色液体,则试剂Y为H2O2,则反应④的总化学方程式为:Cu+H2O2+H2SO4 CuSO4+2H2O;Cu全部溶解且溶液中含铜元素的溶质仅为CuSO4,则化学方程式为:3Cu+2HNO3+3H2SO4
CuSO4+2H2O;Cu全部溶解且溶液中含铜元素的溶质仅为CuSO4,则化学方程式为:3Cu+2HNO3+3H2SO4 3CuSO4++2NO↑+4H2O,
3CuSO4++2NO↑+4H2O, Cu为3mol,则消耗的HNO3为2mol,需该硝酸的体积为:2mol÷1mol?L?1=2L。
Cu为3mol,则消耗的HNO3为2mol,需该硝酸的体积为:2mol÷1mol?L?1=2L。


科目:高中化学 来源:2014高考名师推荐化学CB计算法(解析版) 题型:选择题
某混合溶液中所含离子的浓度如下表,则M离子可能为
所含离子 | NO | SO42- | H+ | M |
浓度(mol·L-1) | 2 | 1 | 2 | 1 |
A.Mg2+ B.Ba2+ C.F- D.Na+
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测7 题型:选择题
下列分类正确的是
A.共价化合物:硫酸、水、纯碱
B. 非电解质:乙醇、二氧化碳、氨气
C. 胶体:饱和氯化铁溶液、豆浆、牛奶
D.硅酸盐产品:水晶、玻璃、陶瓷
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测6 题型:选择题
锅炉水垢是一种安全隐患,除去水垢中的CaSO4,可先用Na2CO3溶液处理,使之转化为易溶于酸的CaCO3,而后用酸除去。下列说法不正确的是:
A.CaCO3的溶解度小于CaSO4
B.沉淀转化的实质是沉淀溶解平衡的移动
C.沉淀转化的难易与溶解度差别的大小无关
D.CaSO4到CaCO3的沉淀转化中并存着两个沉淀溶解平衡
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测6 题型:选择题
已检测出pH=1的某未知溶液中含有Al3+和 ,若检验此溶液中是否大量存在以下6种离子:①ClO- ②
,若检验此溶液中是否大量存在以下6种离子:①ClO- ② ③Fe2+④K+ ⑤
③Fe2+④K+ ⑤ ⑥Cl-,其中不必检验就能加以否定的离子是
⑥Cl-,其中不必检验就能加以否定的离子是
A.①②⑥
B.②③④
C.①③⑤
D.④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测5 题型:选择题
用NA表示阿伏加德罗常数的值。下列叙述中正确的是
A.78 g 苯含有碳碳双键的数目为3NA
B.常温常压下,22.4 L二氧化碳含有的原子总数为3NA
C.1 mol Fe与足量稀HNO3反应,转移3 NA个电子
D.1 L 1 mol·L-1的NaClO 溶液中含有ClO-的数目为NA
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测5 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.1.0mol·L-1的KNO3溶液:Cl-、SO42-、H+、Fe2+
B.c(H+)=1.0×10-12mol·L-1的溶液:K+、Na+、CH3COO-、Br-
C.甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl-
D.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测4 题型:选择题
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:
2X(g)+Y(g) Z(g) △H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是
Z(g) △H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是
A.以Y浓度变化表示的反应速率为0.0005 mol/(L·s)
B.其他条件不变,将容器体积扩大至20 L,则Z的平衡浓度变为原来的1/2
C.其他条件不 变,将容器体积缩小至5L,平衡正向移动,平衡常数增大
变,将容器体积缩小至5L,平衡正向移动,平衡常数增大
D.其他条件不变,升高温度逆反应速率加快,正反应速率减慢
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测17 题型:推断题
化合物A是合成天然橡胶的单体,分子式为C5H8,A的一系列反应如下(部分反应条件略去)

回答下列问题:
(1)A的结构简式为 ,化学名称是 ;
(2)B的分子式为 ;
(3)②的反应方程式为 ;
(4)①和③的反应类型分别是 , ;
(5)C为单溴代物,分子中有两个亚甲基,④的化学方程式为 ;(6)A的同分异构体中不含聚集双烯(C=C=C)结构单元的链状烃还有 种,写出其中互为立体异构体的化合物的结构简式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com