
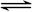 1/2N2O4(g) △H = -26.35 kJ·mol-1
1/2N2O4(g) △H = -26.35 kJ·mol-1
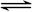 1/2N2O4(g)可知,如果②×2-①-③×2即得到2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g),所以反应热为-534.0 kJ/mol×2-67.7 kJ/mol+26.35 kJ/mol×2="-1083.0" kJ/mol。
1/2N2O4(g)可知,如果②×2-①-③×2即得到2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g),所以反应热为-534.0 kJ/mol×2-67.7 kJ/mol+26.35 kJ/mol×2="-1083.0" kJ/mol。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分子晶体中的每个分子内一定含有极性共价键 |
| B.原子晶体中的相邻原子间只存在非极性共价键 |
| C.含有阴离子的化合物一定含有阳离子 |
| D.金属晶体的熔点和沸点都很高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 化学键 | H—H | H—Cl | H—I | Cl—Cl | Br—Br |
键能/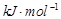 | 436 | 431 | 299 | 247 | 193 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com