
���� ��1���ٸ��ݷ�Ӧ��Ͳ�������ϵ���͵Ĵ�С�����ж��ر���ţ�
�ڸ÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���ƽ�ⳣ����С��
��A�������¶ȣ���ѧ��Ӧ���ʼӿ죬ƽ��������У�
B����CH3OH��g������ϵ�з��룬��ѧ��Ӧ���ʼ�����ƽ�������ƶ���
C������He��ʹ��ϵ��ѹǿ����������䣬�����Ũ�Ȳ��䣬���Ի�ѧ��Ӧ���ʲ��䣬ƽ�ⲻ���ƶ���
D���ٳ���2mol CO��5mol H2������ѹǿ����ѧ��Ӧ���ʼӿ죬ƽ�������ƶ���
�ܻ�ѧ��Ӧ�ﵽ��ѧƽ��״̬ʱ�����淴Ӧ������ȣ��Ҳ�����0�������ʵ�Ũ�Ȳ��ٷ����仯���ɴ�������һЩ�������������仯���Դ˽����жϣ��ó���ȷ���ۣ�
��2���ٸ���CO��ת���ʼ����������ƽ��ʱ�����ʵ�����
�ڸ���ƽ�ⳣ�������������Ũ����֮�����Է�Ӧ���Ũ����֮�����м��㣻
�۸���v=$\frac{��c}{��t}$���м��㣮
��� �⣺��1���ٸ÷�Ӧ�У���Ӧ���ϵ���ʹ��ڲ�������ϵ���ͣ����Ը÷�Ӧ���ؼ��ķ�Ӧ���ر�С���㣬�ʴ�Ϊ������
�ڸ÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���ƽ�ⳣ����С����ƽ�ⳣ��K��T1��С��K��T2�����ʴ�Ϊ��С�ڣ�
��A�������¶ȣ���ѧ��Ӧ���ʼӿ죬ƽ��������У����С�״����ʣ���A����
B����CH3OH��g������ϵ�з��룬��ѧ��Ӧ���ʼ�����ƽ�������ƶ�����״��IJ��ʣ���B����
C������He��ʹ��ϵ��ѹǿ����������䣬�����Ũ�Ȳ��䣬���Ի�ѧ��Ӧ���ʲ��䣬ƽ�ⲻ���ƶ�������ı�״����ʣ���C����
D���ٳ���2mol CO��5mol H2������ѹǿ����ѧ��Ӧ���ʼӿ죬ƽ�������ƶ���������״��IJ��ʣ���D��ȷ��
�ʴ�Ϊ��D��
��CO��g��+2H2��g���TCH3OH��g��
A��v������CH3OH��������Ӧ���ʣ�v������CO��Ҳ�Ƿ�Ӧ���ʣ��ʲ���˵���ﵽƽ��״̬����A����
B���ܶ�=$\frac{������}{���}$�����������䣬������䣬�ʻ��������ܶȲ��䣬�ʻ��������ܶȲ��ٸı䲻��˵���ﵽƽ��״̬����B����
C��ƽ����Է�������=$\frac{������}{�����ʵ���}$�����������䣬�����ʵ�����䣬�ʻ�������ƽ����Է����������ٸı�˵���ﵽƽ��״̬����C��ȷ��
D��CO��H2Ũ�ȱȲ��ٱ仯��˵���ﵽƽ��״̬����D��ȷ��
�ʴ�Ϊ��CD��
��2�������¶�T2ʱ��5min��Ӧ�ﵽƽ�⣬CO��ת����Ϊ75%����Ӧ��CO�����ʵ���Ϊ��2mol��75%=1.5mol����Ӧ�����������ʵ���Ϊ��1.5mol��2=3mol��ƽ��ʱCO�����ʵ���Ϊ��2-1.5=0.5mol�����������ʵ���Ϊ5-3=2mol���״������ʵ���Ϊ1.5mol����ƽ��ʱ��ϵ�ܵ����ʵ���Ϊ0.5+2+1.5=4mol��
�ʴ�Ϊ��4��
��ƽ��ʱCO�����ʵ���Ϊ0.5mol�����������ʵ���Ϊ2mol���״������ʵ���Ϊ1.5mol����ƽ�ⳣ��K=$\frac{c��C{H}_{3}OH��}{c��CO��•{c}^{2}��{H}_{2}��}$=$\frac{\frac{1.5}{10}}{\frac{0.5}{10}��\frac{2}{10}��\frac{2}{10}}$=75L2/mol2��
�ʴ�Ϊ��75L2/mol2��
�۷�Ӧ�����������ʵ���Ϊ3mol����v��H2��=$\frac{\frac{3mol}{10L}}{5min}$=0.06 mol•L-1•min-1���ʴ�Ϊ��0.06 mol•L-1•min-1��
���� ���⿼�黯ѧ��Ӧ���ʵ�Ӱ�����ؼ���ؼ��㣬��ѧƽ���ƶ�ԭ����ƽ���־���жϣ���ѧƽ�ⳣ������ؼ����֪ʶ���Ѷ��еȣ�Ҫע��ƽʱ����֪ʶ�Ļ��ۣ�


 ���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�
���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 8�� | B�� | 12�� | C�� | 24�� | D�� | 64�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
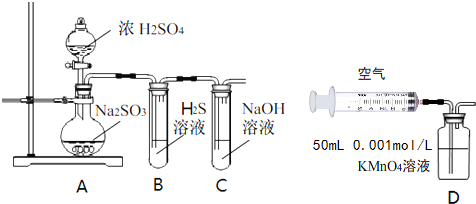
| ʵ�鲽�� | ʵ����� | Ԥ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
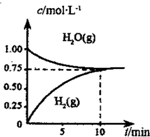 ��ҵ���Ʊ��ϳ����Ĺ�����Ҫ��ˮ�����������飺CH4��g��+H2O��g��?CO��g��+3H2��g����H��0����һ�������£������Ϊ1L���ܱ������г���1mol CH4��g����1mol H2O��g�������H2O��g����H2��g����Ũ����ʱ��仯������ͼ��ʾ������˵����ȷ���ǣ�������
��ҵ���Ʊ��ϳ����Ĺ�����Ҫ��ˮ�����������飺CH4��g��+H2O��g��?CO��g��+3H2��g����H��0����һ�������£������Ϊ1L���ܱ������г���1mol CH4��g����1mol H2O��g�������H2O��g����H2��g����Ũ����ʱ��仯������ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ��ƽ��ʱ��CH4��g����ת����Ϊ75% | |
| B�� | 0��10min�ڣ�v��CO��=0.075mol•L-1•min-1 | |
| C�� | �÷�Ӧ�Ļ�ѧƽ�ⳣ��K=O.1875 | |
| D�� | ��CH4��g��������������H2��g���������������ʱ����Ӧ����ƽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
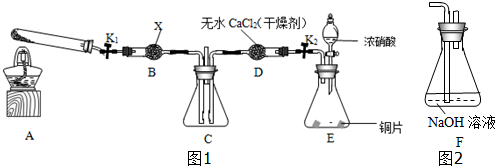
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
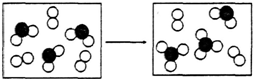 A��B��C��D��E��F��ԭ��������������Ķ�����Ԫ�أ�B�Ƕ������н�������ǿ��Ԫ�أ�C�ǵؿ��к�����ߵĽ���Ԫ�أ�D���ʵľ��������õİ뵼����ϣ�E���������������ڲ������֮��Ϊ3��5��A��Eͬ�壮
A��B��C��D��E��F��ԭ��������������Ķ�����Ԫ�أ�B�Ƕ������н�������ǿ��Ԫ�أ�C�ǵؿ��к�����ߵĽ���Ԫ�أ�D���ʵľ��������õİ뵼����ϣ�E���������������ڲ������֮��Ϊ3��5��A��Eͬ�壮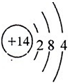
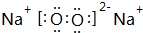 ��
�� Al��OH��3��3H+���������������壬������ˮ�������ʹ֮���۴ﵽ��ˮĿ��
Al��OH��3��3H+���������������壬������ˮ�������ʹ֮���۴ﵽ��ˮĿ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 5��6��7 | B�� | 1��1��1 | C�� | 4��8��5 | D�� | 8��4��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 | |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | �� | ||
| 4 | �� | �� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com