
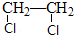 .
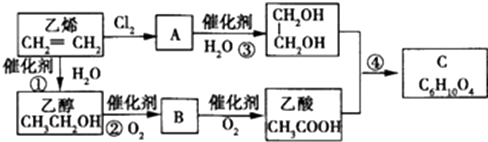
.分析 乙烯与溴发生加成反应生成A为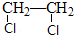 ,A发生水解得乙二醇,乙烯与水发生加成得乙醇,乙醇催化氧化得B为CH3CHO,B氧化得乙酸,根据C的分子式可知,乙酸与乙二醇发生酯化反应得C为CH3COOCH2CH2OOCCH3,据此答题.
,A发生水解得乙二醇,乙烯与水发生加成得乙醇,乙醇催化氧化得B为CH3CHO,B氧化得乙酸,根据C的分子式可知,乙酸与乙二醇发生酯化反应得C为CH3COOCH2CH2OOCCH3,据此答题.
解答 解:乙烯与溴发生加成反应生成A为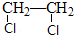 ,A发生水解得乙二醇,乙烯与水发生加成得乙醇,乙醇催化氧化得B为CH3CHO,B氧化得乙酸,根据C的分子式可知,乙酸与乙二醇发生酯化反应得C为CH3COOCH2CH2OOCCH3,
,A发生水解得乙二醇,乙烯与水发生加成得乙醇,乙醇催化氧化得B为CH3CHO,B氧化得乙酸,根据C的分子式可知,乙酸与乙二醇发生酯化反应得C为CH3COOCH2CH2OOCCH3,
(1)B为CH3CHO,其含有的官能团为醛基,C为CH3COOCH2CH2OOCCH3,其含有的官能团为酯基,
故答案为:醛基;酯基;
(2)根据上面的分析可知,A的结构简式为: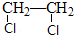 ,
,
故答案为: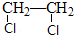 ;
;
(3)由合成流程图可知,反应①为乙烯与水的加成反应生成乙醇,反应③为1,2-二溴乙烷发生水解反应生成乙二醇,
故答案为:加成;水解;
(4)乙酸的属于酯的同分异构体的结构简式为HCOOCH3,
故答案为:HCOOCH3;
(5)反应②为乙醇催化氧化生成乙醛,反应方程式为:2CH3CH2OH+O2$\frac{\underline{\;催化剂\;}}{△}$2CH3CHO+2H2O,
反应④为乙二醇与乙酸发生酯化反应生成C,由C的分子式可知,应是1分子乙二醇与2分子乙酸反应,则C为二乙酸乙二酯(CH3COOCH2CH2OOCCH3),反应方程式为:2CH3COOH+HOCH2-CH2OH$→_{△}^{浓硫酸}$CH3COOCH2-CH2OOCCH3+2H2O,
故答案为:2CH3CH2OH+O2$\frac{\underline{\;催化剂\;}}{△}$2CH3CHO+2H2O;2CH3COOH+HOCH2-CH2OH$→_{△}^{浓硫酸}$CH3COOCH2-CH2OOCCH3+2H2O;
(6)B与新制Cu(OH)2悬浊液反应的化学方程式为CH3CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH3COONa+Cu2O↓+3H2O,
故答案为:CH3CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH3COONa+Cu2O↓+3H2O.
点评 本题考查有机物的推断与合成,难度中等,在注重对学生基础知识巩固的同时,培养学生的知识的迁移能力,记住常见官能团的结构、性质以及官能团之间的相互转化是关键,注意合成路线中碳原子数目的变化.


科目:高中化学 来源: 题型:解答题
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、Cl-、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 浓度 时间(秒) 反应条件 | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
| MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
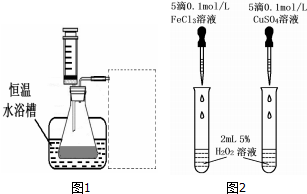
| 所需试剂 | 操作及现象 | 结论 |
| Cl对H2O2分解无催化作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 元素代号 | G | L | M | Q | R | T |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.104 | 0.075 | 0.066 |
| 主要化合价 | +1 | +2 | +3 | +6,-2 | +5,-3 | -2 |
| A. | GOH溶液和M(OH)3可以相互反应 | B. | 非金属性:T<Q | ||
| C. | 气态氢化物的稳定性:R>T | D. | L2+与T2-核外电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验事实 | 理论解释 |
| A | 氧化性:HClO>HClO4 | HClO4分子中非羟基氧原子数目较多 |
| B | 沸点:SiO2>CO2 | 相对分子质量越大沸点越高 |
| C | 密度:干冰>冰 | 干冰晶体属于分子密堆积 |
| D | 分解温度:MgO>NaCl | MgO晶格能大于NaCl |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | P、S、Cl元素最高化合价依次升高 | |
| C. | N、O、F原子半径依次增大 | |
| D. | P、S、Cl元素的最低化合价依次为-3、-2、-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为CH2=C(CH3)CH2C(CH3)3或(CH3)2C=CH(CH3)3.
它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为CH2=C(CH3)CH2C(CH3)3或(CH3)2C=CH(CH3)3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A易溶于某些有机溶剂 | B. | A的氢化物很不稳定 | ||
| C. | A是有色气体 | D. | A化银不溶于水或稀HNO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com