
| A. | 25$°\\;C$C、101KPa下,NA个C18O2分子的质量为48g | |
| B. | 标准状况下,22.4L HF中含有的电子数为10NA | |
| C. | 1mol H3+O所含的电子数是11NA | |
| D. | 1L 0.1mol/L的NaClO水溶液中含有的氧原子数为0.1NA |
分析 A.n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$计算分析;
B.标况下,HF是液态;
C.H3O+所含电子数为10;
D.水中也含O原子;
解答 解:A.NA个C18O2分子物质的量为1mol,其的质量=1mol×48g/mol=48g,故A正确;
B.标准状况下,22.4L HF物质的量不是1mol,故B错误;
C.1mol H3O+所含的电子数是10NA,故C错误;
D.水中含O原子,则溶液中含有的氧原子数远大于0.1NA,故D错误;
故选A.
点评 本题考查物质的量计算及阿伏伽德罗常数,为高频考点,把握物质的量的相关计算公式、物质的组成、氧化还原反应等为解答的关键,侧重分析与计算能力的考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 通入HCl气体之前:c(S2-)>c(HS-)>c(OH-)>c(H+) | |
| B. | pH=7的溶液中:c(Cl-)═c(HS-)+2c(H2S) | |
| C. | c(HS-)=c(S2-)的碱性溶液中:c(Cl-)+c(HS-)>0.100 mol•L-1+c(H2S) | |
| D. | c(Cl-)=0.100 mol•L-1的溶液中:c(OH-)-c(H+)=c(H2S)-c(S2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
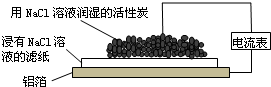
| A. | 铝箔为正极,发生氧化反应而被腐蚀 | |
| B. | 负极反应为2H2O+O2+4e-═4OH- | |
| C. | Cl-由活性炭区向铝箔表面区迁移,铝箔表面有氯气产生 | |
| D. | 白斑的主要成分可能是Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用过量氨水吸收工业尾气中的SO2:NH3•H2O+SO2═NH4++HSO3- | |
| B. | 氯化钠固体与浓硫酸混合加热:2H++H2SO4+2Cl-$\frac{\underline{\;△\;}}{\;}$SO2↑+Cl2↑+2H2O | |
| C. | 氧化亚铁溶于稀硝酸:3 Fe2++4H++NO3-═3Fe3++NO↑+2H2O | |
| D. | 0.01 mol•L-1 NH4Al(SO4)2溶液与0.02 mol•L-1Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
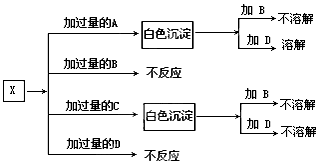 A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种.现利用另一种溶液X,用如下图所示的方法即可将它们确定.
A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种.现利用另一种溶液X,用如下图所示的方法即可将它们确定.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1>△H2>△H3 | B. | △H2>△H3>△H1 | C. | △H2>△H1>△H3 | D. | △H3>△H2>△H1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com