
一定温度下,用水稀释0.1 mol/L的一元弱酸HA,随稀释进行,下列数值一定增大的是(KW 表示水的离子积,Ka表示HA的电离常数)( )
表示水的离子积,Ka表示HA的电离常数)( )
A.KW B.
C.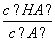 D.c(OH-)
D.c(OH-)
科目:高中化学 来源: 题型:
一定条件下存在反应:CO(g)+H2O(g)CO2(g)+H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO和2 mol H2O,700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
A.容器Ⅰ、Ⅱ中正反应速率相同
B.容器Ⅰ、Ⅲ中反应的平衡常数相同
C.容器Ⅰ中CO的物质的量比容器Ⅱ中的多
D.容器Ⅰ中CO的转化率与容器Ⅱ中CO2的转化率之和小于1
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)(4分)物质的量是一个联系宏观和微观的物理量。填写关于物质的量计算的四个恒等式(NA表示阿伏加德罗常数):
n= = = = 。
(2)(5分)同温同压下,同体积的N2和SO2分子数之比为 ,物质的量之比为 ,原子总数之比为 ,摩尔质量之比为 ,质量之比为 。
(3)(1分)若某原子的摩尔质量为M g·mol-1,则一个该原子的真实质量是__________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于0.10 mol·L-1 NaHCO3溶液的说法正确的是( )
A.溶质的电离方程式为NaHCO3===Na++H++CO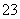
B.25 ℃时,加水稀释后,n(H+)与n(OH-)的乘积变大
C.离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HCO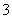 )+c(CO
)+c(CO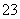 )
)
D. 温度升高,c(HCO )增大
)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列三种溶液中,由水电离出的氢离子浓度之比为( )
①1 mol/L 的盐酸 ②0.1 mol·L-1的盐酸
③0.01 mol·L-1的NaOH
A.1∶10∶100 B.0∶1∶12
C.14∶13∶12 D.14∶13∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中与1.0× 10-5 mol·L-1的NaOH溶液的pH相同的是( )
10-5 mol·L-1的NaOH溶液的pH相同的是( )
A.把pH=6的盐酸稀释1 000倍
B.把pH=10的Ba(OH)2溶液稀释10倍
C.把pH=8和pH=10的NaOH溶液等体积混合
D.把pH=8的NaOH溶液稀释10倍
查看答案和解析>>
科目:高中化学 来源: 题型:
用标准的KOH溶液滴 定未知浓度的盐酸,若测定结果偏低,其原因可能是( )
定未知浓度的盐酸,若测定结果偏低,其原因可能是( )
A.配制标准溶液的固体KOH中混有NaOH杂质
B.滴定终点读数时,俯视滴定管的刻度,其他操作正确
C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗
D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,在0.2 mol·L-1 Al2(SO4)3溶液中,逐滴加入1.0 mol·L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积的变化曲线如图所示,下列有关说法正确的是( )
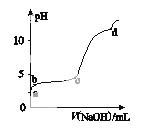
A.a点时,溶液呈酸性的原因是Al3+水解,离子方程式为Al3++3OH- Al(OH)3
Al(OH)3
B.a~b段,溶液pH增大,Al3+浓度不变
C.b~c段,加入的OH-主要用于生成Al(OH)3沉淀
D.d点时,Al(OH)3沉淀开始溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电离方程式错误的是
A.CaCl2 =Ca2++2Cl- B.Ba(OH)2=Ba2++2OH-
C.HNO3=H++NO3- D.NaHCO3=Na++H++CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com