
【题目】废水、废气、废渣的处理是减少污染、保护环境的重要措施.
(1)烟气中的NOx必须脱除(即脱硝)后才能排放. ①列举一种由NOx引起的大气污染现象: .
②已知:CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=﹣890.3kJmol﹣1
N2(g)+O2(g)═2NO(g);△H=+180kJmol﹣1
则CH4脱硝的热化学方程式为CH4(g)+4NO(g)═CO2(g)+2N2(g)+2H2O(l),△H= .
③图1是一种用NH3脱除烟气中NO的原理.该脱硝反应中,氧化剂是;
(2)图2是一种三室微生物燃料电池污水净化系统原理示意图,同时处理有机废水和硝酸盐废水,并获得淡水.图中有机废水中有机物可用C6H10O5表示. 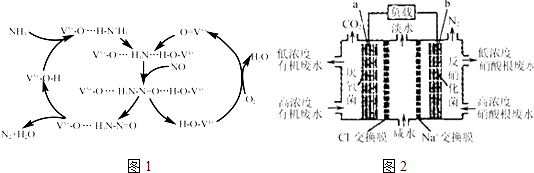
①电池正极为 . (填“a”或“b”)
②电极a上的电极反应式为 .
③电池工作过程中Na+离子移向、Cl﹣离子移向 . (填“a电极”、或“b电极”)
④假设咸水中氯化钠的质量分数为2.34%,当两极总共产生7.84L气体(标准状况下)时,理论上处理咸水g.(忽略CO2的溶解)
【答案】
(1)光化学烟雾(或硝酸型酸雨);﹣1250.3 kJ?mol﹣1;NO
(2)b;C6H10O5﹣24e﹣+7H2O═6CO2↑+24H+;b电极;a电极;2500
【解析】解:(1)①光化学烟雾(或硝酸型酸雨)都是氮的氧化物引起的,所以答案是:光化学烟雾(或硝酸型酸雨);②已知:①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890.3kJmol﹣1 , ②N2(g)+O2(g)═2NO(g)△H=+180kJmol﹣1根据盖斯定律:①﹣2×②得CH4(g)+4NO(g)═CO2(g)+2N2(g)+2H2O(l),△H=﹣890.3kJmol﹣1﹣2×(+180kJmol﹣1)=﹣1250.3 kJmol﹣1;
所以答案是:﹣1250.3 kJmol﹣1;③氮的化合价降低,所以氧化剂是一氧化氮,所以答案是:NO;(2)该原电池中,硝酸根离子得电子发生还原反应,则右边装置中电极b是正极,电极反应式为2NO3﹣+10e﹣+12H+=N2↑+6H2O,左边装置电极a是负极,负极上有机物失电子发生氧化反应,有机物在厌氧菌作用下生成二氧化碳,电极反应式为C6H10O5﹣24e﹣+7H2O═6CO2↑+24H+ , ①该原电池中,硝酸根离子得电子发生还原反应,电极反应式为2NO3﹣+10e﹣+12H+=N2↑+6H2O,则右边装置中电极b是正极,所以答案是:b;②左边装置电极a是负极,负极上有机物失电子发生氧化反应,有机物在厌氧菌作用下生成二氧化碳,电极反应式为C6H10O5﹣24e﹣+7H2O═6CO2↑+24H+ , 所以答案是:C6H10O5﹣24e﹣+7H2O═6CO2↑+24H+;③放电时,电解质溶液中阳离子Na+移向正极右室即向b电极,阴离子Cl﹣移向负极室左室即a电极,所以答案是:b电极;a电极;④整个电路转移120mol电子时,负极生成30mol的二氧化碳气体,正极生成12mol的氮气,除理氯化钠120mol,得到关系式为:
42mol气体~ | 120molNaCl, |
42×22.4 | 120×58.5 |
7.84 | 2.34%×m |
则42×22.4×2.34%×m=7.84×120×58.5,解之得x=2500g,所以答案是:2500.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法,错误的是( )
A.过氧化钠可用作潜水艇里氧气的来源B.甲醛可用作食物的防腐剂
C.柠檬黄可作食品添加剂中的着色剂D.小苏打可用作食品的疏松剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人建议将氢元素排在元素周期表的ⅦA族。下列事实能支持这一观点的是( )。
①H原子得到一个电子实现最外电子层稳定结构;
②氢分子的结构式为H—H;
③与碱金属元素形成离子化合物:M+[:H]-
④分子中原子间的化学键都属于非极性键
A. ①②③ B. ①③④ C. ②③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.10molL﹣1盐酸分别滴定20.00mL 0.10molL﹣1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示.下列说法不正确的是( ) 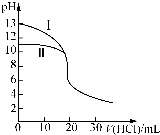
A.Ⅱ 表示的是滴定氨水的曲线,当V(HCl)=20 mL时,有:c(Cl﹣)>c(NH4+)>c(H+)>c(OH﹣)
B.当pH=7时,滴定氨水消耗的V(HCl)=20 mL,且c(NH4+)=c(Cl﹣)
C.滴定氢氧化钠溶液时,若V(HCl)>20 mL,则一定有:c(Cl﹣)>c(Na+)>c(OH﹣)>c(H+)
D.当滴定氨水消耗V(HCl)=10 mL时,有:2[c(OH﹣)﹣c(H+)]=c(NH4+)﹣c(NH3H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A.所有的非金属元素都分布在P区
B.除氦外的稀有气体原子的最外层电子数都是8
C.原子的核外电子层数等于该元素所在的周期数
D.元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中混有的少量杂质(括号内为杂质),所用试剂或方法错误的是
物质(杂质) | 除杂试剂或方法 | |
A | CO2(SO2) | NaOH溶液 |
B | 汽油(H2O) | 分液 |
C | FeCl3溶液(FeCl2) | Cl2 |
D | Na2CO3固体(NaHCO3) | 加热 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 王水是浓硝酸和浓盐酸按物质的量之比为1:3组成的混合物
B. pH小于5.6的雨水称为酸雨
C. 分散质粒子直径介于1nm~100nm之间的分散系称为胶体
D. 光导纤维的主要成分是SiO2,太阳能光电池板的主要成分是硅晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A,B,C,D四种短周期主族元素,它们的原子序数依次增大,其中A元素原子核外电子仅有一种原子轨道,也是宇宙中最丰富的元素,B元素原子的核外p轨道电子数比s轨道电子数少1,C为金属元素且原子核外p轨道电子数和s轨道电子数相等,D元素的原子核外所有p轨道全充满或半充满.
(1)写出C,D两种基态原子核外电子排布图:C;D .
(2)写出B元素单质和氢化物的电子式:单质 , 氢化物 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com