
【题目】下列说法正确的是( )
A. 离子化合物中不可能有共价键
B. 共价化合物中可能有离子键
C. 凡含有离子键的化合物就一定是离子化合物
D. 只含有共价键的物质一定是共价化合物
科目:高中化学 来源: 题型:
【题目】利用海水提取溴和镁的过程如下,下列说法不正确的是( ) 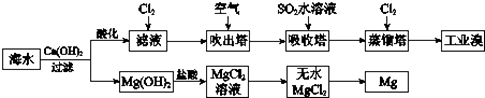
A.工业溴中含少量Cl2 , 可用NaOH溶液除去
B.工业上常利用电解熔融MgCl2冶炼金属镁
C.富集溴元素过程中,空气吹出法利用了溴易挥发的性质
D.若提取1 mol Br2 , 至少需要标准状况下44.8 L的Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东汉成书的《神农本草经》有“石胆化铁为铜”(石胆是硫酸铜)的记载。这一方法开创了人类文明史上湿法冶金的先河。其中涉及的化学反应类型是
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往100 mL 1 mol·L -1 的AlCl3 溶液中滴加1 mol·L -1 的NaOH溶液,得3.9 g沉淀,则加入NaOH溶液的体积可能是
A. 100 mL B. 200 mL C. 300 mL D. 350 mL
【答案】D
【解析】氯化铝的物质的量是0.1mol,生成的氢氧化铝是3.9g÷78g/mol=0.05mol,如果氯化铝过量,则根据Al3++3OH-===Al(OH)3↓可知需要氢氧化钠是0.15mol,溶液体积是0.15mol÷1mol/L=0.15L=150mL;如果氢氧化钠过量,生成的氢氧化铝部分溶解,则0.1mol氯化铝需要0.3mol氢氧化钠生成0.1mol氢氧化铝,其中有0.05mol氢氧化铝溶解,根据Al(OH)3+OH-===AlO2-+2H2O可知又需要0.05mol氢氧化钠,则溶液体积是0.35mol÷1mol/L=0.35L=350mL,答案选D。
点睛:该题也可以借助图像解答,例如把强碱溶液逐滴加入到铝盐(Al3+)溶液中至过量的现象是:先有白色沉淀产生,然后沉淀逐渐溶解,有关反应:A→B:Al3++3OH-===Al(OH)3↓、B→D:Al(OH)3+OH-===AlO2-+2H2O,图像: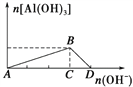 ,作纵坐标的垂线与图像有2个交点(B点除外),因此需要氢氧化钠的物质的量也有两种情况,解答时可以灵活应用。
,作纵坐标的垂线与图像有2个交点(B点除外),因此需要氢氧化钠的物质的量也有两种情况,解答时可以灵活应用。
【题型】单选题
【结束】
11
【题目】某溶液中有Fe3+、Mg2+ 、Fe2+ 和Al3+ 四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量增加的阳离子是
A. Fe3+ B. Mg2+ C. Fe2+ D. Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物不能由CH2=CH2通过加成反应制取的是( )
A. CH3CH2ClB. CH2Cl—CH2Cl
C. CH3—CH2OHD. CH3—COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:I2+2S2O32﹣═S4O62﹣+2I﹣
相关物质的溶度积常数见下表:
物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10﹣20 | 2.6×10﹣39 | 1.7×10﹣7 | 1.3×10﹣12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3 , 为得到纯净的CuCl22H2O晶体,加入 , 调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)= . 过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl22H2O晶体.
(2)在空气中直接加热CuCl22H2O晶体得不到纯的无水CuCl2 , 原因是(用化学方程式表示).由CuCl22H2O晶体得到纯的无水CuCl2的合理方法是 .
(3)某学习小组用“间接碘量法”测定含有CuCl22H2O晶体的试样(不含能与I﹣发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀.用0.100 0molL﹣1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用作滴定指示剂,滴定终点的现象是 .
②CuCl2溶液与KI反应的离子方程式为 .
③该试样中CuCl22H2O的质量百分数为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法错误的是( )
A.20℃时,铝的密度为2.7 g/cm3 , 则1个Al原子的体积为( ![]() )cm3
)cm3
B.25℃、101KPa下,16 g O2与O3的混合气体中含电子数为8NA
C.25℃、101KPa下,11.2L Cl2含有的分子数小于0.5NA
D.0℃、101KPa下,等体积的CH4和CCl4中含C原子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要 0.2mol/L的硫酸铜溶液480ml,现用胆矾晶体来配制该溶液,回答下列问题
(1)实验中用到的玻璃仪器有量筒、玻璃棒、烧杯、托盘天平,还缺少(填仪器名称)
(2)应称量胆矾晶体的质量 .
(3)下列操作会使所配溶液浓度偏低的是 .
①胆矾失去了部分结晶水②容量瓶未干燥就使用③称量晶体时所用的砝码已经生锈④定容时俯视刻度线⑤定容摇匀后发现液面低于刻度线,又加水至刻度线
(4)下列操作中,容量瓶所不具备的功能有(填序号).
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
(5)若实验室想要将密度为1.84g/cm3、质量分数为98%的浓硫酸稀释成1000ml、物质的量浓度为2mol/L、密度为1.20g/cm3的稀硫酸,则所需浓硫酸的体积 , 所需水的体积 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com