
| Fe3+ | Al3+ | Fe2+ | |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 |
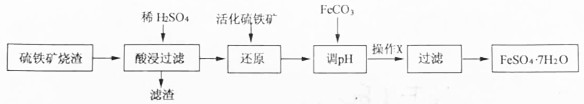
分析 硫铁矿烧渣加入硫酸酸浸,得到滤渣为SiO2,滤液中含有硫酸铁、硫酸亚铁以及硫酸铝等,加入活化硫铁矿还原得到滤液含有硫酸亚铁、硫酸铝,调节溶液pH5.2~6.5之间可除去铝离子,过滤、蒸发浓缩、冷却结晶得到FeSO4•7H2O晶体.
解答 解:硫铁矿烧渣加入硫酸酸浸,得到滤渣为SiO2,滤液中含有硫酸铁、硫酸亚铁以及硫酸铝等,加入活化硫铁矿还原得到滤液含有硫酸亚铁、硫酸铝,调节溶液pH5.2~6.5之间可除去铝离子,过滤、蒸发浓缩、冷却结晶得到FeSO4•7H2O晶体.
(1)酸浸过程中金属氧化物都和稀盐酸反应生成氯化物,主要离子反应方程式为Fe2O3+6H+=2Fe3++3H2O,滤渣为SiO2,
故答案为:Fe2O3+6H+=2Fe3++3H2O;SiO2;
(2)如含有铁离子,加入KSCN发生颜色反应,溶液呈红色,则可用KSCN检验,故答案为:C;
(3)加FeCO3调节溶液pH至5.2~6.5之间,可除去铝离子,且防止生成氢氧化亚铁沉淀,故答案为:5.2~6.5;除去铝离子,防止生成氢氧化亚铁沉淀;
(4)加入碳酸亚铁固体之后,应充分搅拌,使之充分反应,然后静置浊液,过滤,以得到硫酸亚铁溶液,故答案为:搅拌;静置.
点评 本题考查制备实验方案设计,为高考高频点,此种题型涉及物质性质、实验基本操作,明确物质的性质及每一步发生的反应、基本操作方法是解本题关键,熟练掌握元素化合物知识,灵活运用知识解答问题,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | NaHSO3溶液中投入过氧化钠粉末:4HSO3-+2Na2O2═4SO32-+O2↑+4Na+ | |
| B. | 明矾溶液与等物质的量的氢氧化钡溶液混合:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ | |
| C. | 氢氧化钙溶液与碳酸氢镁溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O | |
| D. | 将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-=Fe3++2H2O+NO↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol任何物质都含有6.02×1021个原子, | |
| B. | 0.012kg12C含有6.02×1023碳原子 | |
| C. | 阿伏伽德罗常数表示的粒子“集体”就是1mol | |
| D. | 使用摩尔这一单位时必须指明粒子的名称 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
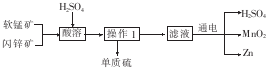
| A. | 酸溶时,ZnS作氧化剂 | B. | 硫酸可以循环使用 | ||
| C. | 可用盐酸代替硫酸进行酸溶 | D. | MnO2和ZnS均属于盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
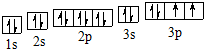 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见如图,电池总反应可表示为:2H2+O2═2H2O,下列有关说法正确的是( )
某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见如图,电池总反应可表示为:2H2+O2═2H2O,下列有关说法正确的是( )| A. | 电子通过外电路从b极流向a极 | |
| B. | b极上的电极反应式为:O2+4H++4e-═2H2O | |
| C. | 每转移0.1mol电子,消耗1.12L的H2 | |
| D. | H+由b极通过固体酸电解质传递到a极 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com