
| ||
| ||


科目:高中化学 来源: 题型:
| A、只有②③ | B、只有①③ |
| C、只有①④ | D、只有②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
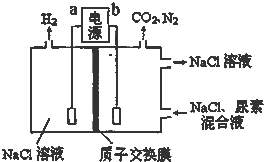 用如图装置模拟人工肾脏的工作原理,电解生成的Cl2将尿素[CO(NH2)2]氧化成N2排出,则下列说法错误的是( )
用如图装置模拟人工肾脏的工作原理,电解生成的Cl2将尿素[CO(NH2)2]氧化成N2排出,则下列说法错误的是( )| A、电解结束后,阴极室溶液与电解前相比pH增大 |
| B、尿素被氧化的化学方程式为CO(NH2)2+3Cl2+H2O=N2+CO2+6HCl |
| C、电源的正极为b |
| D、电解结束后,若两极共收集到气体13.44 L(标准状况)时,则被氧化的尿素为7.2 g(忽略气体的溶解) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2S比H2O的沸点低的原因是H2O分子间存在氢键 |
| B、氯化氢极易溶于水是因为氯化氢溶于水时形成了氢键 |
| C、氨易液化与氨分子间存在氢键无关 |
| D、H2O是一种非常稳定的化合物,这是由于氢键所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同压强、同体积的N2O和CO2 |
| B、同温度、同体积的氮气和氯气 |
| C、同体积、同密度的乙烯和丙烯 |
| D、同温度、同压强、同体积的氦气和氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向含1mol碘化亚铁的溶液中通入标况下44.8L氯气:2Fe2++2I-+2Cl2=2Fe3++2I2+4Cl- |
| B、铝铵矾[NH4Al(SO4)2?12H2O]溶液中加入过量Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| C、H2O2溶液中滴加酸性KMnO4溶液:2 MnO4-+5 H2O2+6H+=2Mn2++5O2↑+8H2O |
| D、NaHCO3溶液水解的离子方程式为:HCO3-+H2O?CO32-+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③④ | B、①④ |
| C、①②③④ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
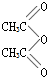 ,
,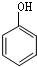 +AS
+AS| H+ |
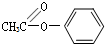 +CH3COOH
+CH3COOH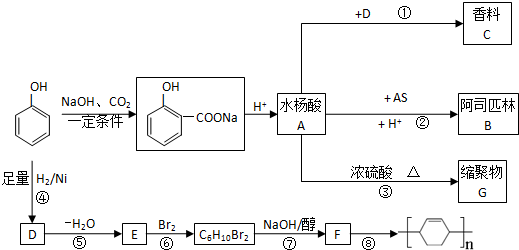
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com