
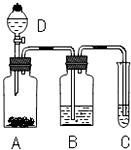
 某学生为了验证苯酚、醋酸、碳酸的酸性强弱,设计了实验装置:回答下列问题:
某学生为了验证苯酚、醋酸、碳酸的酸性强弱,设计了实验装置:回答下列问题: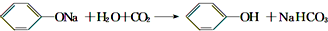 .
. 分析 将CH3COOH与Na2CO3发生反应:Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑,说明酸性CH3COOH>H2CO3;产生的CO2气体先通过饱和的碳酸氢钠溶液除去混有的醋酸蒸汽,然后再通入苯酚钠溶液发生反应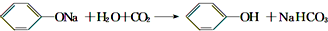 ,说明酸性H2CO3>
,说明酸性H2CO3>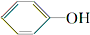 ,据此回答.
,据此回答.
解答 解:将CH3COOH与Na2CO3发生反应:Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑,说明酸性CH3COOH>H2CO3;产生的CO2气体通入苯酚钠溶液发生反应: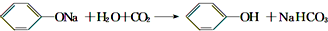 说明酸性H2CO3>
说明酸性H2CO3> ;
;
(1)D中为醋酸,滴加到A中与Na2CO3反应生成二氧化碳,B中为饱和碳酸氢钠溶液,除去二氧化碳中混有的醋酸蒸汽,二氧化碳与通入C中与苯酚钠反应生成苯酚;
故答案为:④;⑥;②;
(2)产生的CO2气体中混有醋酸蒸汽,会干扰二氧化碳与苯酚钠的反应,所以用饱和的碳酸氢钠溶液除去二氧化碳中混有的醋酸蒸汽;
故答案为:除去二氧化碳中混有的醋酸蒸汽;
(3)CH3COOH与Na2CO3发生反应生成CO2,产生的CO2通入苯酚钠溶液,发生反应: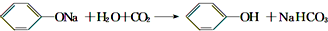 ,
,
故答案为: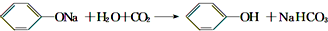 .
.
点评 本题考查了探究顺序强弱实验,明确物质的性质是解本题关键,结合强酸制取弱酸实验原理来分析解答,注意:醋酸有挥发性,导致制取的二氧化碳中含有醋酸,干扰实验,为易错点.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤⑧ | B. | ④⑤⑦⑧ | C. | ④⑤⑧ | D. | ③④⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
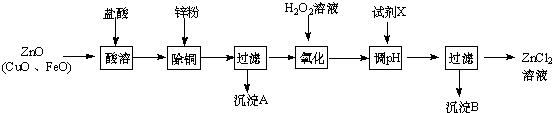
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.2 | 6.4 |
| Fe2+ | 5.8 | 8.8 |
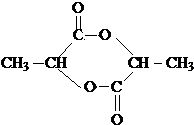 ,聚乳酸的结构简式为
,聚乳酸的结构简式为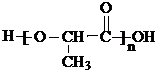 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
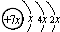 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题: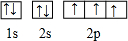
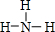 ,其中心原子D的杂化方式为sp3.
,其中心原子D的杂化方式为sp3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 测试时间段 | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
| 序号 | 二氧化硫的性质 | 主要操作和现象 | 化学方程式 |
| ① | 将二氧化硫通入装有品红溶液的 试管中,品红由红色变为无色 | ||
| ② | 将二氧化硫与硫化氢气体混合,出现 黄色固体. | SO2+2H2S=3S+2H2O | |
| ③ | 将二氧化硫通入装有新制氯水的试管中,氯水由浅黄绿色变为无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作 | 目的 | |
| A | 食醋浸泡水垢 | 比较乙酸和碳酸的酸性强弱 |
| B | 向蔗糖溶液中加入稀硫酸,水浴加热,5min后向其中加入新制Cu(OH)2的悬浊液,加热. | 证明蔗糖水解产物中有葡萄糖 |
| C | 向NaBr溶液中加入少量氯水,振荡后加入少量四氯化碳,振荡,静置. | 比较氯、溴非金属性强弱 |
| D | 钠分别与水和乙醇反应 | 乙醇羟基中氢原子不如水分子中氢原子活泼 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com