
下列说法正确的是
A.CH3COOH与CH3COONa混合溶液中,一定有c(CH3COO-) >c(Na+)
B.向新制氯水中加入CaCO3可使溶液中HClO浓度增大
C.AgCl在200ml 0.1mol/LNaCl中的溶解度小于在50ml 0.1mol/LMgCl2中溶解度
D.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
科目:高中化学 来源: 题型:
糖尿病是由于人体内胰岛素紊乱导致的代谢紊乱综合征,以高血糖为主要标志。长期摄入高热量食品或缺少运动,都会导致糖尿病。
(1)血糖是指血液中的葡萄糖,下列有关说法正确的是______________。(2分)
A.葡萄糖分子可表示为C6(H2O)6,则每个葡萄糖分子含有6个H2O分子
B.葡萄糖与果糖互为同分异构体
C.糖尿病人尿糖较高,可用新制的氢氧化铜来检测人尿液中的葡萄糖
D.淀粉水解的最终产物是氨基酸
(2)糖尿病人不可过量饮酒,将会一定程度上造成胰岛细胞损伤。但酒精在肝脏内可转化成有机物A。A的实验结果如下:
① 通过实验测得A的相对分子质量为60;
② A由C、H、O三种元素组成,分子中只存在两种类型的氢原子,且这两种类型的氢原子个数比为1∶3
③ A可与酒精在一定条件下生成有芳香气味的物质。
纯净的A又称为______________,结构简式为____________________。(2分)
A的主要化学性质有(用化学方程式表示):a____________________________________,
b___________________________________________。(4分)
查看答案和解析>>
科目:高中化学 来源: 题型:
透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶。制备它的一种配方中含有下列四种物质:
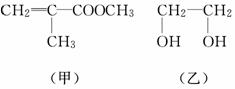
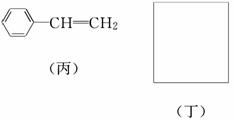
填写下列空白:
(1)甲中不含氧原子的官能团是________;下列试剂能与甲反应而褪色的是________(填标号)。
a.Br2/CCl4溶液 b.石蕊溶液
c.酸性KMnO4溶液
(2)甲的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式:________。
(3)淀粉通过下列转化可以得到乙(其中A~D均为有机物):
淀粉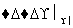 A
A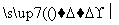 B
B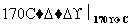 C
C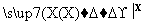 D
D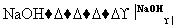 乙
乙
A的分子式是________,试剂X可以是________。
(4)已知:
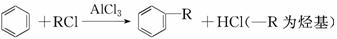
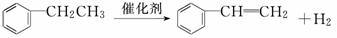
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是__________________________________________________________
________________________________________________________________________。
(5)化合物丁仅含碳、氢、氧三种元素,相对分子质量为110。丁与FeCl3溶液作用显现特征颜色,且丁分子中烃基上的一氯取代物只有一种。则丁的结构简式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知一种c(H+)=1×10-3 mol·L-1的酸溶液和一种c(OH-)=1×10-3 mol·L-1的碱溶液等体积混合后,溶液呈酸性,其原因可能是( )
A.浓的强酸和稀的强碱溶液反应 B.浓的弱酸和稀的强碱溶液反应
C.等浓度的强酸和弱碱溶液反应 D.生成了一种强酸弱碱盐
查看答案和解析>>
科目:高中化学 来源: 题型:
(Ⅰ)某二元酸(H2A)在水中的电离方程式是:H2A===H++HA-,HA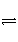
 -H++A2-。
-H++A2-。
(1)Na2A溶液显________(填“酸性”、“中性”或“碱性”)。理由是
________________________________________________________________________
(用离子方程式表示)。
(2)已知0.1 mol/L NaHA溶液的pH=2,则0.1 mol/L H2A溶液中氢离子的物质的量浓度应______0.11 mol/L(填“<”、“>”或“=”),理由是
________________________________________________________________________
________________________________________________________________________。
(Ⅱ)25℃时,A酸溶液的pH=a,B碱溶液的pH=b。
(1)若A为强酸,B为强碱,且a+b=14,若两者等体积混合后,溶液的pH=________,此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是
________________________________________________________________________。
(2)若A的化学式为HR,B的化学式为MOH,且a+b=14,两者等体积混合后溶液显酸性,则混合溶液中必定有一种离子能发生水解,该离子为__________(填离子符号);混合后的溶液中,下列微粒浓度大小关系一定正确的是____________(填序号)。
①c(MOH)>c(M+)>c(R-)>c(H+)>c(OH-)
②c(HR)>c(M+)>c(R-)>c(OH-)>c(H+)
③c(R-)>c(M+)>c(H+)>c(OH-)
④c(M+)>c(R-)>c(OH-)>c(H+)
⑤c(M+)+c(H+)=c(R-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
硅、硫、钠、铁、铝、铜等元素及其化合物在日常生活和生产中应用广泛,回答下列问题:
(1)Si元素在周期表中的位置是 , Na2S的电子式为 。
(2)H2S 、H2O 、SiO2、Na2O熔沸点由高到低的顺序为 。(用化学式表示)
(3)工业上常用氯化铁溶液腐蚀铜制电路板,反应的离子方程式是 。
要从上述腐蚀液中获得较纯的CuCl2溶液,需要将杂质 FeCl3和FeCl2除去,首先将Fe2+氧化成Fe3+,再向溶液中加入 (填化学式),最后过滤。
(4)在CuSO4溶液中通入过量的NH3,小心蒸发,最终得到[ Cu(NH3)4]SO4 晶体,晶体中含有的化学键除普通的共价键外,还含有 。
(5)将4.6g Na和8.1gAl组成的混合物投入到足量的水中,生成H2在标准状况下的体积为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.Na与H2O的反应是熵增的放热反应,该反应能自发进行
B.饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同
C.FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同
D.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s) Mg2+(aq)+2OH—(aq),该固体可溶于NH4Cl溶液
Mg2+(aq)+2OH—(aq),该固体可溶于NH4Cl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡: CO(g)+H2S(g) COS(g)+H2(g) K=0.1
COS(g)+H2(g) K=0.1
反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是( )
A.升高温度,H2S浓度增加,表明该反应是吸热反应
B.通入CO后,正反应速率逐渐增大
C.反应前H2S物质的量为7mol
D.CO的平衡转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
热化学方程式C(s)+H2O(g)===CO(g)+H2(g) ΔH=+131.3 kJ·mol-1表示( )
A.碳和水反应吸收131.3 kJ能量
B.1 mol碳和1 mol水反应生成1 mol一氧化碳和1 mol氢气并吸收131.3 kJ热量
C.1 mol固态碳和1 mol水蒸气反应生成1 mol一氧化碳气体和1 mol氢气并吸收131.3 kJ热量
D.1个固态碳原子和1分子水蒸气反应吸热131.3 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com