
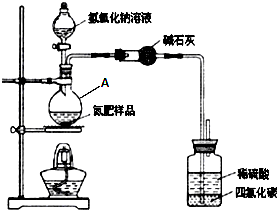
 某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组设计的实验装置图如图.请回答相关问题:
某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组设计的实验装置图如图.请回答相关问题:

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不用试剂 | B、1种 |
| C、2种 | D、3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| NaOH、H2O |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2SO3溶液与BaCl2溶液混合有白色沉淀生成,加稀HNO3沉淀不消失 |
| B、将SO2气体通入足 量Ba(OH)2溶液中有白色沉淀生成,加足 量HCl后沉淀消失 |
| C、将SO2气体通入BaCl2溶液中有白色沉淀生成,加稀HCl后沉淀消失 |
| D、将SO2气体通入氯水中无沉淀生成,加入BaCl2溶液有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(HCOO-)<c(Na+) |
| B、c(HCOO-)>c(Na+) |
| C、c(HCOO-)=c(Na+) |
| D、c(Na+)=c(HCOO-)+c(HCOOH) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com