
| A. | 稀盐酸 | B. | KSCN溶液 | C. | 铁粉 | D. | 石蕊试液 |
分析 如果FeCl2溶液变质,变质后的溶液中一定含有FeCl3,Fe3+能和SCN-生成络合物,溶液呈现血红色,据此进行解答.
解答 解:A.FeCl2不与稀盐酸反应,无法鉴别氯化亚铁是否变质,故A错误;
B、如果FeCl2溶液变质,变质后的物质是FeCl3,Fe3+能和SCN-生成络合物,使溶液呈现血红色,这一反应是Fe3+的特征反应,所以用KSCN溶液可以检验FeCl2溶液是否变质,故B正确;
C.铁片与氯化亚铁不反应,无法鉴别,故C错误;
D.无论氯化亚铁是否变质,都是强酸弱碱盐,溶液都呈酸性,所以无法用石蕊试液检验,故D错误;
故选B.
点评 本题考查了铁离子、亚铁离子的检验方法,题目难度不大,明确铁离子、亚铁离子的性质及检验方法为解答关键,注意掌握检验Fe3+的常用试剂:KSCN(溶液变血红色)、苯酚(溶液呈紫色)、NaOH等.


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铝是白色胶状沉淀,能凝聚水中的悬浮物,但不能吸附色素 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大题水冲洗,然后涂上硼酸 | |
| C. | 氮气化学性质通常不活泼,可将炽热的镁粉可放在氮气中冷却 | |
| D. | 酒精灯着火时可用水扑灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场 | |
| B. | 氢气在盛有氯气的集气瓶中燃烧,瓶口有白烟产生 | |
| C. | 氯气能与铁反应,液氯不宜贮存在钢瓶中 | |
| D. | 工业上以氯气和澄清石灰水为原料制造漂白粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 切开的金属Na暴露在空气中,光亮表面逐渐变暗2Na+O2═Na2O2 | |
| B. | 少量铜片放入浓硝酸中,有红棕色气体生成:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| C. | Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物2Na2O2+2CO2═2Na2CO3+O2 | |
| D. | 向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,27g Al3+中含有的电子数目为13 NA | |
| B. | 22.4 L氧气中一定含有2NA个氧原子 | |
| C. | 23gNa和足量的O2完全燃烧条件下转移电子数为NA | |
| D. | 标准状况下,22.4 L乙醇(CH3CH2OH)中含有的氧原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 |
| A | 加热放在坩埚中的小块钠 | 钠先熔化成光亮的小球,燃烧时,火焰为黄色,燃烧后,生成淡黄色固体 |
| B | 在酒精灯上加热铝箔 | 铝箔熔化,失去光泽,熔化的铝并不滴落, 好像有一层膜兜着 |
| C | 点燃的镁条伸入盛有O2的集气瓶(底部铺有少量细砂)中 | 镁条继续燃烧,发出耀眼白光放出大量热量,生成白色固体 |
| D | 在空气中久置的铝条放入NaOH溶液中 | 立刻产生大量无色气泡,铝条逐渐变细, 铝条逐渐发热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
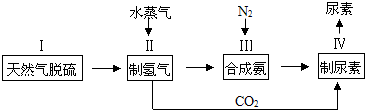
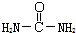 ,请写出尿素的同分异构体中含有离子键的化学式NH4OCN.
,请写出尿素的同分异构体中含有离子键的化学式NH4OCN.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com