
【题目】柠檬酸铁铵[(NH4)3Fe( C6 H5O7)2,摩尔质量488 g/mol] 是一种重要的食品添加剂。一种制备柠檬酸铁铵的实验步骤如下:

步骤1.在右图三颈烧瓶中加入16.7 g FeSO4·7H2O、40 ml.蒸馏水,3mL硫酸和1 g NaClO3,强力搅拌;
步骤2.升温至80℃,再补加l g NaClO3;
步骤3.向反应器中加入NaOH溶液,温度控制在80~90℃,剧烈搅拌;
步骤4.过滤,洗涤,沥干,得活性Fe(OH)3;
步骤5.将Fe(OH)3和一定量的水加入三颈烧瓶中,控制95℃以上,加入计算量的柠檬酸溶液,搅拌,并保温1h;
步骤6.冷却到50℃,搅拌下加入氨水40 mL,静置、浓缩至膏状,80℃干燥得柠檬酸铁铵24.9 g。
回答下列问题:
(1)步骤1发生反应的离子方程式为_____________________________。
(2)步骤2再补加NaClO3的目的是_____________________________。
(3)步骤3确定Fe3+已沉淀完全的方法是_____________________________。
(4)步骤4过滤时,所需硅酸盐质仪器除烧杯外,还需要_____________________________;证明Fe(OH)3已被洗涤干净的方法为__________________________。
(5)柠檬酸铁铵的产率为_________(结果保留三位有效数字)。
【答案】 6Fe2++ClO3-+6 H+=6Fe3++Cl- +3H2O 确保Fe2+全部转化为Fe3+ 在上层清液中继续滴加NaOH溶液,不产生沉淀(或其他合理答案) 漏斗和玻璃棒 取最后一次洗涤液于两支试管中,分别滴加氯化钡或硝酸银溶液,并用硝酸酸化,均无白色沉淀出现,证明Fe(OH)3已被洗涤干净 85.0%
【解析】(1)步骤1是氯酸钠在酸性条件下氧化硫酸亚铁,发生反应的离子方程式为6Fe2++ClO3-+6 H+=6Fe3++Cl- +3H2O。
(2)步骤2再补加NaClO3的目的是确保Fe2+全部转化为Fe3+ 。
(3)步骤3确定Fe3+已沉淀完全的方法是,在上层清液中继续滴加NaOH溶液,不产生沉淀。
(4)步骤4过滤时,所需硅酸盐质仪器除烧杯外,还需要漏斗和玻璃棒;证明Fe(OH)3已被洗涤干净的方法为取最后一次洗涤液于两支试管中,分别滴加氯化钡或硝酸银溶液,并用硝酸酸化,均无白色沉淀出现,证明Fe(OH)3已被洗涤干净。
(5)16.7 g FeSO4·7H2O的物质的量约为0.06mol,在理论上能制备0.06mol(NH4)3Fe( C6 H5O7)2,0.0601mol(NH4)3Fe( C6 H5O7)2的质量为29.3g,所以柠檬酸铁铵的产率为![]() 85.0% 。
85.0% 。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】金和铜可以形成多种金属化合物,其中一种晶体的结构如图所示(为面心立方体结构). 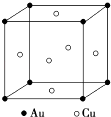
(1)该金属化合物的化学式为 .
(2)已知Au 的相对原子质量为197,Cu的相对原子质量为64,阿伏加德罗常数为NA , 若该化合物的密度为dgcm﹣3 , 试计算面上距离最近的两个金原子的核间距为cm.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在绿色化学工艺中,理想状态是反应物中的原子全部转化为欲制得的产物,即原子利用率为100%,在用CH3C≡CH合成CH2=C(CH3)COOCH3的过程中,欲使原子利用率达到最高,还需要其他的反应物有
A. CO2和H2O B. CO和CH3OH C. CH3OH和H2 D. H2和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列有关说法正确的是 ( )
A. 糖类、蛋白质、油脂都属于天然高分子化合物
B. 油脂是产生能量最高的营养物质
C. 石油裂化的主要目的是为了获得芳香烃
D. 煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分开
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完全燃烧一定质量的无水乙醇,放出的热量为Q,已知为了完全吸收生成的二氧化碳,消耗50mL 8mol/L的氢氧化钠溶液,则无水乙醇的燃烧放出的热量不可能是( )
A. 10Q B. 5Q~10Q C. 大于10Q或小于5Q D. 小于8Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容. 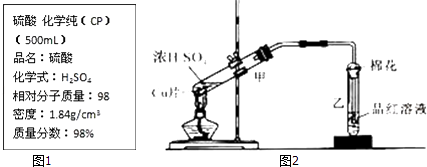
(1)Ⅰ.硫酸具有A﹣D所示的性质,以下过程主要表现了浓硫酸的那些性质?请将选项字母填在下列各小题的括号内:
A酸性 B 吸水性 C 脱水性 D 强氧化性
①浓硫酸可以干燥氢气
②浓硫酸使木条变黑
③热的浓硫酸与铜片反应
④浓硫酸使胆矾变为白色
(2)Ⅱ.现用该浓硫酸配制100mL 1mol/L的稀硫酸.可供选用的仪器有:
①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平.
请回答下列问题:
(i)配制稀硫酸时,上述仪器中不需要使用的有(选填序号),还缺少的玻璃仪器有(写仪器名称);
(ii)经计算,配制100mL1mol/L的稀硫酸需要用量筒量取上述浓硫酸的体积为mL(保留一位小数).
(3)Ⅲ、如图2为浓硫酸与铜片反应的装置.请回答:
①浓硫酸与铜片反应的化学方程式为 .
②反应一段时间后,试管乙中品红溶液的现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第ⅢA族Al、Ga均为两性元素,Al(OH)3与Ga(OH)3相比,后者酸性比前者强。当CO2通入NaAlO2和NaGaO2的溶液中,首先沉淀出来的氢氧化物是( )
A.Al(OH)3B.Ga(OH)3C.同时沉淀D.无法判断
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com