
| A、H3O+和OH- |
| B、CH3+和NH4+ |
| C、CO和N2 |
| D、HNO2和NO2- |


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
| A、蒸馏实验中,要在烧瓶中加入几粒沸石或碎瓷片,以防止液体暴沸 |
| B、手持试管给试管里的物质加热 |
| C、将浓硫酸倒入盛水的量筒中稀释 |
| D、用嘴吹灭酒精灯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、29:8 | B、22:1 |
| C、13:8 | D、8:13 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molNH3所含有的原子数为NA |
| B、常温常压下,22.4L氧气所含的原子数为2NA |
| C、常温常压下,48gO3所含的氧原子数为3NA |
| D、标准状况下,33.6LH2O含有9.03×1023个H2O分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2属于温室气体 |
| B、太阳能电池可将太阳能直接转化为电能 |
| C、太阳能属于新能源 |
| D、乙醇属不可再生能源,乙醇燃烧不会产生温室气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属氧化物一定是碱性氧化物 |
| B、非金属氧化物一定是酸性氧化物 |
| C、只有在标准状况下,气体的摩尔体积才能为22.4L/mol |
| D、非电解质在水溶液中和熔融状态下均以分子形式存在,因而不能导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
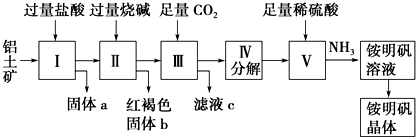
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、检验食盐中含有钠离子,可以用焰色反应实验,如果焰色呈黄色则可以说明含有钠离子 |
| B、检验食盐中含有氯离子,则可以加用硝酸酸化的硝酸银溶液 |
| C、向溴水中加入食盐溶液,可以使溴水褪色 |
| D、食盐中加碘的作用是预防“大脖子病”的发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 生理盐水,是指生理学实验或临床上常用的渗透压与动物或人体血浆的渗透压相等的氯化钠溶液.浓度:用于两栖类动物时是0.67~0.70%,用于哺乳类动物和人体时是0.85~0.9%人们平常点滴用的氯化钠注射液浓度是0.9%,可以当成生理盐水来使用.请回答下面有关点滴用的氯化钠注射液的问题.
生理盐水,是指生理学实验或临床上常用的渗透压与动物或人体血浆的渗透压相等的氯化钠溶液.浓度:用于两栖类动物时是0.67~0.70%,用于哺乳类动物和人体时是0.85~0.9%人们平常点滴用的氯化钠注射液浓度是0.9%,可以当成生理盐水来使用.请回答下面有关点滴用的氯化钠注射液的问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com