
A、..向某无色溶液中加入BaCl2溶液有白色沉淀出现,再加入稀盐酸,沉淀不消失,则该溶液中一定含有SO
| ||
| B、.检验Na2CO3固体中是否混有NaHCO3,可向固体滴加稀盐酸,观察是否产生气体 | ||
| C、.焰色反应试验中,透过蓝色钴玻璃,可观察到Na+离子火焰呈黄色 | ||
| D、用丁达尔效应可鉴别FeCl3溶液和Fe(OH)3胶体 |


科目:高中化学 来源: 题型:
| A、①②⑤ | B、③④⑤ |
| C、②④⑥ | D、③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、③④ | C、②③ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaCN |
| 水 |
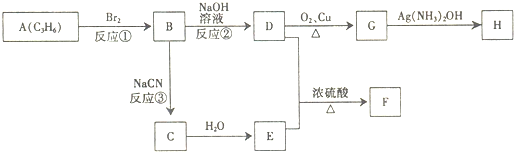
查看答案和解析>>
科目:高中化学 来源: 题型:
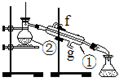
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验方案 | 实验现象与结论 |
| 取少量干燥的蓝绿色固体于试管中, |
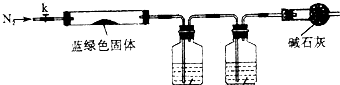
查看答案和解析>>
科目:高中化学 来源: 题型:
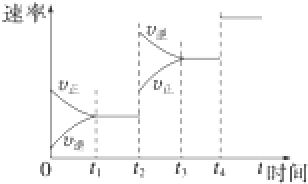
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com