
以下说法正确的是()
A.某吸热反应能自发进行,因此该反应是熵增反应
B.常温下Na与足量O2反应生成Na2O随温度升高生成Na2O的速率逐渐加快
C.放热反应速率总是大于吸热反应速率
D.1gH2完全燃烧生成水蒸气时放出热量为121kJ,完全断裂1mol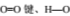 键吸收热量为496kJ、463kJ,则断裂1mol H-H键时吸收热量为902kJ
键吸收热量为496kJ、463kJ,则断裂1mol H-H键时吸收热量为902kJ
A
【解析】
试题分析:A. 某吸热反应能自发进行,根据体系的自由能ΔG=ΔH-TΔS<0,可以自发进行可知:该反应是熵增反应,正确;B. 常温下Na与足量O2反应生成Na2O,当温度升高后不仅该反应速率会增加,还会发生反应产生Na2O2,错误;C. 影响化学反应速率的大小的因素有很多,当可逆反应达到平衡时放热反应速率等于吸热反应速率,错误;D. 反应热是断键吸热与成键放热的差值。1gH2完全燃烧生成水蒸气时放出热量为121kJ,若完全断裂1molO=O键、H—O键吸收热量为496kJ、463kJ,则断裂1mol H-H键时吸收热量为[-121kJ×4+(4×463kJ )-496kJ ]÷2=436kJ,错误。
考点:考查反应的自发性、键能与反应热的关系、反应原理与温度及反应的热效应与温度的关系的知识。


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源:2015届安徽省江淮十校高三11月联考化学试卷(解析版) 题型:选择题
氢化铝钠(NaAlH4)是最有研究应用前景的络合金属氢化物,氢化铝钠储放氢时发生反应:3NaAlH4 Na3AlH6+2Al+3H2↑。下列说法正确的是
Na3AlH6+2Al+3H2↑。下列说法正确的是
A.NaAlH4中含有离子键和非极性共价键
B.每生成11. 2 L(标准状况下)H2,转移NA个电子
C.NaAlH4中氢元素为+1价,在反应中有50%的氢被还原
D.反应中氧化产物与还原产物的物质的量之比为1:1
查看答案和解析>>
科目:高中化学 来源:2015届宁夏高三年级第二次月考理综化学试卷(解析版) 题型:选择题
磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性,制备时将含等物质的量的FeSO4和Fe2(SO4)3的溶液混合,再滴入稍过量的NaOH溶液,随后加入油酸钠溶液,即可生成黑色的、分散质粒子直径在36~55 nm的磁流体。下列说法中正确的是
A.所得的分散系属于悬浊液
B.该分散系能产生丁达尔效应且其中胶粒带正电荷
C.所得的分散系中分散质为Fe2O3
D.所得分散系为胶体,且胶粒直径即为氢氧化铁分子直径
查看答案和解析>>
科目:高中化学 来源:2015届天津一中高三化学9月考化学试卷(解析版) 题型:选择题
下列说法不正确的是()
A.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
B.用甘氨酸和丙氨酸缩合最多可形成4种二肽
C.分子式为C5H8O2,既能与Na2CO3溶液反应又能与溴的四氯化碳溶液反应的有机物有8种
D.乳酸薄荷醇酯(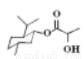 )仅能发生水解、氧化、消去反应
)仅能发生水解、氧化、消去反应
查看答案和解析>>
科目:高中化学 来源:2015届天津一中高三化学9月考化学试卷(解析版) 题型:选择题
X、Y、Z、W代表原子序数依次增大的四种短周期元素。在周期表中Z与Y相邻,Z与W也相邻,Y、Z和W三种元素的原子最外层电子数之和为17,X能分别与Y、Z形成电子总数相等的分子A、B。下列有关判断正确的是()
A.原子半径由大到小的顺序为:W>Z>Y
B.两种钠盐都含有 X、Z、W三种元素,它们之间可发生化学反应
C.X、Y、Z、W的原子形成的化合物中只存在共价键
D.化合物B中含有的化学键为非极性共价键
查看答案和解析>>
科目:高中化学 来源:2015届天津一中高三化学9月考化学试卷(解析版) 题型:选择题
下列说法正确的是()
A.同体积、同密度的C2H4和C3H6所含原子数一定相等
B.同主族元素的最高正价都相同
C.CH3COONa和NaOH中化学键类型完全相同
D. 最外层有5个电子的原子都是非金属原子
查看答案和解析>>
科目:高中化学 来源:2015届四川省2015届高三9月理综化学试卷(解析版) 题型:实验题
(14分)工业上生产金属钛的方法很多。以钛铁矿(主要成分FeTiO3,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如下,其中钛铁矿与浓硫酸发生反应的化学方程式为:
FeTiO3+2H2SO4=TiOSO4+FeSO4+2H2O
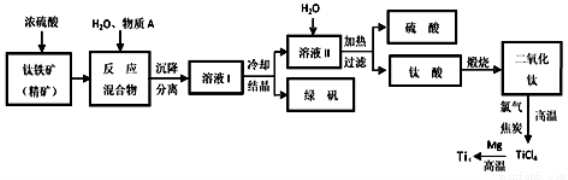
回答下列问题:
(1)钛铁矿和浓硫酸反应属于_________(选填“氧化还原反应”或“非氧化还原反应”)。
(2)上述生产流程中加入物质A的目的是防止Fe2+被氧化,物质A是________,上述制备TiO2的过程中,所得到的副产物和可回收利用的物质分别是__________、___________。
(3)反应TiCl4+2Mg=2MgCl2+Ti在Ar气氛中进行的理由是_____________________。
(4)由二氧化钛制取四氯化钛所涉及的反应有:
TiO2 (s)+ 2Cl2 (g) +2C(s) =TiCl4(g) + 2CO(g)
ΔH1 = -72 kJ?mol-1 TiO2(s) + 2Cl2 (g) =TiCl4(g) + O2 (g)
ΔH2 =+38.8kJ?mol-1
C(s)+CO2(g)=2CO(g)? ΔH3 =+282.8kJ?mol-1
①反应C(s)+CO2(g)=2CO(g)在高温下能够自发进行
的原因是______________________。
②反应C(s)+O2(g)=CO2 (g)的ΔH=_______________。
(5)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO
作电解质,利用下图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。
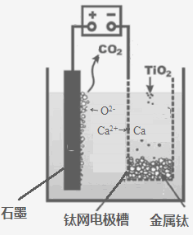
①写出阳极所发生反应的电极反应式:_______________________。
②在制备金属钛前后,CaO的总量不变,其原因是(请结合化学用语解释) _________。
查看答案和解析>>
科目:高中化学 来源:2015届四川省高三第三次理综考试化学试卷(解析版) 题型:选择题
五种短周期元素的某些性质如下表所示:
元素代号 | X | W | Y | Z | Q |
原子半径(×10-12 m) | 37 | 99 | 66 | 104 | 154 |
主要化合价 | +1 | -1、+7 | -2 | -2、+6 | +1 |
下列说法正确的是( )
A.由Q与Y形成的化合物中只存在离子键
B.Z与X之间形成的化合物具有还原性
C.X、Y元素组成的化合物的沸点高于X、Z元素组成化合物的沸点是由于Y非金属性比Z强
D.Y、Q、W三种元素组成化合物的水溶液一定显碱性
查看答案和解析>>
科目:高中化学 来源:2015届四川省绵竹市高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列离子方程式不正确的是
A.醋酸溶液中加入少量氢氧化镁固体:Mg(OH)2+2CH3COOH═Mg2++2CH3COO﹣+2H2O
B.H2O2溶液中加入足量酸性KMnO4溶液:2MnO4﹣+3H2O2+6H+═2Mn2++6H2O+4O2↑
C.Ca(HCO3)2溶液中加入足量澄清石灰水:Ca2++HCO3﹣+OH﹣═CaCO3↓+H2O
D.NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至SO42﹣恰好沉淀完全:NH4++H++SO42﹣+Ba2++2OH﹣=NH3?H2O+BaSO4↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com