
| A、最外层电子数是核外电子总数的1/5的原子和价电子排布式为4s24p5的两个微粒属于同种元素的原子 |
| B、在一个基态的多电子的原子中,不能有两个能量完全相同的电子 |
| C、原子核外的M层上的S能级和P能级都填满电子,而d轨道上尚未有电子的两种原子一定属于同一周期 |
| D、PCl3、BeCl2、BF3中所有原子均满足最外层8电子结构 |
| 1 |
| 5 |
| 1 |
| 5 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、H2B的电离方程式为:H2B?2H++B2- |
| B、结合质子能力由强到弱的顺序为:B2->A->HB- |
| C、等物质的量浓度NaA、NaHB、Na2B三种盐的水溶液,NaA碱性最强 |
| D、等pH的HA、H2B两种溶液中,水的电离出的氢离子前者大于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:
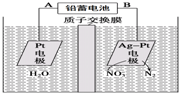
| A、铅蓄电池的A极为正极,电极材料为PbO2 |
| B、铅蓄电池工作过程中负极质量增加 |
| C、该电解池的阴极反应为:2NO3-+6H2O+10e-=N2↑+12OH- |
| D、若电解过程中转移2moL电子,则交换膜两侧电解液的质量变化差(△m左-△m右)为10.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应NH3(g)+HCl(g)?NH4C1(s)△H<O在任何条件下均能自发进行 |
| B、对于可逆反应N2(g)+3H2(g)?2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增加 |
| C、将A1C13溶液和NaAlO2溶液分别蒸干后灼烧,所得固体产物均为A1203 |
| D、恒容密闭容器中进行的反应3A(g)?B(g)+c(g),在其他条件不变的情况下,再充入一定量的A气体,A的转化率将增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将10 g CaCO3粉末加入100 mL水中,所得溶液的浓度为l mol?L-1 |
| B、将100 mL 2 mol?L-1盐酸加热蒸发至50 mL,所得溶液的浓度为4 mol?L-1 |
| C、将l0 mL l.0mol?L-1NaCl溶液与90mL水混合,所得溶液的浓度为0.1 mol?L-1 |
| D、将10 g CaO加入100 mL饱和石灰水中,充分搅拌、静置并恢复到原来的温度,所得溶液的浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100mL 0.5mol/L KClO3溶液 |
| B、200mL 2.5mol/L MgCl2溶液 |
| C、300mL 2mol/L AlCl3溶液 |
| D、400mL1mol/L 盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入合金的质量可能为3.2g |
| B、参加反应的硝酸的物质的量为0.4mol |
| C、沉淀完全时消耗NaOH的物质的量为0.3mol |
| D、还原产物的体积范围2.24L<V还原产物<6.72L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com