
某烯烃的结构简式为
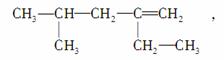
有甲、乙、丙、丁四位同学分别将其命名为:2甲基4乙基4戊烯;2异丁基1丁烯;2,4二甲基3己烯;4甲基2乙基1戊烯,下面对4位同学的命名判断正确的是( )
A.甲的命名中主链选择是错误的
B.乙的命名中对主链碳原子的编号是错误的
C.丙的命名中主链选择是正确的
D.丁的命名是正确的
科目:高中化学 来源: 题型:
写出符合要求的化学方程式或离子方程式:
(1)实验室用二氧化锰和浓盐酸制备氯气的离子方程式_______________________________。
(2)用苯制备硝基苯的化学方程式____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
由铝土矿(主要成分是Al2O3)炼制铝的工艺流程示意图如下:

(1)电解生成的铝在熔融液的 (填“上层”或“下层”),电解时不断消耗的电极是 (填“阴极”或“阳极”)。
(2)写出通入过量二氧化碳酸化时反应的离子方程式: 。
(3)电解制 备铝时,需加入冰晶石(Na3AlF6),其作
备铝时,需加入冰晶石(Na3AlF6),其作 用是 ,工业上可以用氟化氢气体、氢氧化铝和纯碱在高温条件下发生反应来制取冰晶石,写出该反应的化学方程式: 。
用是 ,工业上可以用氟化氢气体、氢氧化铝和纯碱在高温条件下发生反应来制取冰晶石,写出该反应的化学方程式: 。
(4)上述工艺所得铝中往往含有少量Fe和Si等杂质,可用电解方法进一步提纯,该电解池的阴极材料是 (填化学式),阳极的电极反应为  。
。
(5)对金属制品进行抗腐蚀处理,可延长其使用寿命。
①控制一定条件进行电解(见下图),此时铝表面可形成耐酸的致密氧化膜,其电极反应为 ;

②钢材镀铝后,能防止钢材腐蚀,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知维生素A的结构简式如图所示,关于它的说法正确的是( )

A.维生素A是一种酚
B.维生素A具有环己烷的结构单元
C.维生素A的一个分子中有3个双键
D.维生素A的一个分子中有30个氢原子
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式为C2H4O2的结构可能有 和
和 两种,为对其结构进行物理方法鉴定,可用______________或________________。
两种,为对其结构进行物理方法鉴定,可用______________或________________。
(1)若为 ,则红外光谱中应该有____个振动吸收;核磁共振氢谱中应该有__________个峰。
,则红外光谱中应该有____个振动吸收;核磁共振氢谱中应该有__________个峰。
(2)若为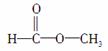 ,则红外光谱中有______个振动吸收;核磁共振氢谱中应有______个峰。
,则红外光谱中有______个振动吸收;核磁共振氢谱中应有______个峰。
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,常用于水的消毒以及纺织高漂白。过氧化氢法生产亚氯酸钠的流程图如下
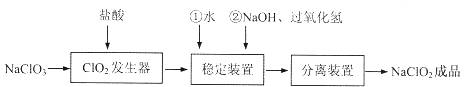
已知NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O且NaClO2在碱性条件下稳定性较高。试回答下列问题:
(1)在ClO2发生器中同时有氯气产生,则在发生器中发生反应的化学方程式为
(2)在NaClO2稳定装置中,H2O2作 (选填序号)。
A.氧化剂 B.还原剂
C.既作氧化剂又作还原剂 D.既不作氧化剂也不作还原剂
(3)在实验室模拟“固体分离装置”中的技术,必须进行的实验操作是 (按实验后顺序填写操作代号)。
A.过滤 B.加热 C.分液 D.蒸馏 E.冷却
(4)经查阅资料知道:当pH≤2.0时,ClO-2能被I完全还原成Cl—;
溶液中Na2S2O3能与I2反应生成NaI和Na2S4O6。
欲测定成品中NaClO2的含量,现进行如下操作:

①步骤Ⅱ中发生反应的离子方程式是 ,
步骤Ⅲ中达到滴定终点时的现象是 。
②若上述滴定操作中用去了V mL Na2S2O3溶液,则样品中NaClO2的质量分数 (用字母表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学学习小组设计如图实验装置(夹持装置略去)制备Cl2,并探究氯气的相关性质.
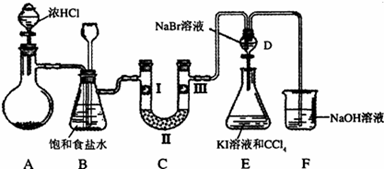
(1)若A装置中固体药品为MnO2,其化学方程式为
若A装置中固体药品为KClO3,则反应中每生成1molCl2时转移电子的物质的量为 mol.
(2)装置B的作用:
(3)装置C的作用是验证氯气是否具有漂白性,l处是湿润的有色布条,则Ⅱ、Ⅲ处应加入的物质分别是 .
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。但有同学认为该设计不够严密,他的理由可能 。
(5)请用化学方程式说明装置F的作用 。
(6)甲同学提出,装置F中的试剂可改用过量的Na2SO3溶液,乙同学认真思考后认为此法不可行.请用离子方程式解释乙认为不可行的原因:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com