
【题目】下列物质中,不能使溴的四氯化碳溶液和高锰酸钾酸性溶液褪色的是( )
A.C2H4B.丙烯C.C5H12D.乙炔
科目:高中化学 来源: 题型:
【题目】在pH=13的无色透明溶液中,能大量共存的离子组为( )
A. HCO3-、Al3+、Na+、SO42- B. I-、NO3-、K+、NH4+
C. SiO32-、OH-、SO32-、Na+ D. MnO4-、Cl-、SO42-、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
对甲苯丙烯酸甲酯 (E)是一种用于合成抗血栓药的中间体,其合成路线如下:
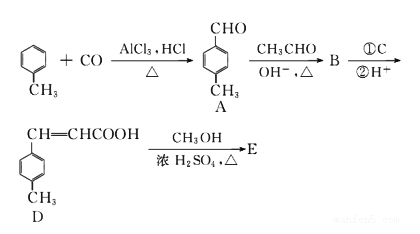
已知:HCHO+CH3CHO![]() CH2=CHCHO+H2O
CH2=CHCHO+H2O
(1)A中官能团的名称为_______,A分子中核磁共振氢谱各峰值比为________。
(2)物质B的结构简式为_______,生成E的反应类型为__________。
(3)试剂C可选用下列中的_________。
a.溴水 b.银氨溶液 c.酸性KMnO4溶液 d.新制Cu(OH)2悬浊液
(4)![]() 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为__________________。
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为__________________。
(5)遇FeCl 3溶液显紫色,且苯环上有两个取代基的A的同分异构体有______种,E在一定条件下可以生成高聚物F,F的结构简式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述正确的是
①CS2为V形的极性分子②ClO3-的立体构型为平面三角形
③SF6中有6对完全相同的成键电子对④SiF4和SO32-的中心原子均采用sp3杂化
A.①③B.②④C.①②D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作,预测的实验现象和实验结论或解释正确的是
实验操作 | 预测的实验现象 | 实验结论或解释 | |
A | 向饱和Na2CO3 溶液中滴加少量稀盐酸 | 立即有气体逸出 | CO32-+2H+=H2O+CO2↑ |
B | 将浓硫酸滴加到盛有铜片的试管中,并将蘸有品红溶液的试纸置于试管口 | 品红试纸褪色 | SO2具有漂白性 |
C | 铝箔在酒精灯火焰上加热 | 铝熔化但不会滴下 | A12O3的熔点比铝高 |
D | 向淀粉的酸性水解液中滴入少量新制 Cu (OH)2悬浊液并加热 | 有砖红色沉淀生成 | 葡萄糖具有还原性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 金刚石、石墨、C60互为同素异形体,它们都是分子晶体
B. 二氧化碳分子和水分子中所有原子在同一条直线上
C. 正丁烷和异丁烷的分子式都为C4H10,它们互为同分异构体
D. 14C与14N互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、恒容下,有反应2A(g)+2B(g)![]() C(g)+3D(g),现从两条途径分别建立平衡。途径Ⅰ:A、B的起始浓度均为2mol·L-1;途径Ⅱ:C、D的起始浓度分别为2mol·L-1和6mol·L-1。以下叙述正确的是( )
C(g)+3D(g),现从两条途径分别建立平衡。途径Ⅰ:A、B的起始浓度均为2mol·L-1;途径Ⅱ:C、D的起始浓度分别为2mol·L-1和6mol·L-1。以下叙述正确的是( )
A. 达到平衡时,途径Ⅰ的反应速率等于途径Ⅱ的反应速率
B. 达到平衡时,途径Ⅰ所得混合气体的压强等于途径Ⅱ所得混合气体的压强
C. 两途径最终达到平衡时,体系内各组分的百分含量相同
D. 两途径最终达到平衡时,体系内各组分的百分含量不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固定容积为2 L的密闭容器中发生反应xA(g)+yB(g)![]() zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图像判断,下列结论正确的是
zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图像判断,下列结论正确的是

A. 200℃时,反应从开始到平衡的平均速率v(A)=0.08molL-1min-1
B. 200℃时,若在第6 min再向体系中充入1 mol He,此时v(正)>v(逆)
C. 若0~5 min内容器与外界的热交换总量为m kJ,则该反应的热化学方程式可表示为:2A(g)+B(g)![]() C(g) ΔH= +5m kJ/mol
C(g) ΔH= +5m kJ/mol
D. 200℃时,平衡后再充入2 mol C,则再次达到平衡时,C的体积分数等于0.25
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com