
| A. | 放电时PbO2为正极,反应的离子方程式为:PbO2+4H++2e-+SO42-═PbSO4+2H2O | |
| B. | 充电时Pb电极为阴极,反应的离子方程式为:PbSO4+2e-═Pb+SO42- | |
| C. | 放电时电解质溶液密度不断减小,可根据电解液密度来判断是否需要充电 | |
| D. | 充电时可直接使用交流电源,不需要充电器也可充入 |
分析 根据电池反应式知,放电时为原电池,铅失电子发生氧化反应而作负极,电极反应式为Pb-2e-+SO42-=PbSO4,二氧化铅得电子作正极,电极反应式为PbO2+SO42-+2e-+4H+═PbSO4+2H2O;充电时为电解池原理,阴极发生的反应是PbSO4+2e-=Pb+SO42-,阳极反应为PbSO4-2e-+2H2O=PbO2+SO42-+4H+,结合电极方程式解答该题.
解答 解:A.放电时为原电池,PbO2得电子作正极,电极反应式为PbO2+SO42-+2e-+4H+═PbSO4+2H2O,故A正确;
B.充电时为电解池原理,Pb电极为阴极,阴极发生的反应是PbSO4+2e-=Pb+SO42-,故B正确;
C.放电时电池总反应Pb+PbO2+2H2SO4═2PbSO4+2H2O,生成水,溶液密度减小,可根据电解液密度来判断是否需要充电,故C正确;
D.充电时用的是直流电源,而不是交流电源,故D错误;
故选D.
点评 本题考查了常见化学电源的基本原理,要求理解原电池和电解池的工作原理,侧重于学生的分析能力的考查,为高频考点,注意根据元素化合价变化确定正负极、阴阳极,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 酒精中是否含有水,可用金属钠检验 | |
| B. | 乙酸乙酯和食用植物油均可水解生成乙醇 | |
| C. | 葡萄糖作为营养剂为人体提供能量,在体内发生氧化反应 | |
| D. | 乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | n+8 | B. | n+16 | C. | n+18 | D. | n+32 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的能量一定低于M的能量,Y的能量一定低于N的能量 | |
| B. | 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 | |
| C. | X和Y的总能量一定低于M和N的总能量 | |
| D. | 因为该反应为吸热反应,故反应一定要加热才能进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
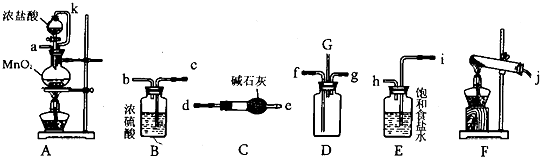
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原混合溶液中c(K+)为2 mol•L-1 | |
| B. | 上述电解过程中共转移2 mol电子 | |
| C. | 向电解后得到的体系中加1molCu2(OH)2CO3固体,可使溶液恢复至电解前的浓度 | |
| D. | 电解后溶液中c(H+)为2 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中的c(OH-)为1×10-10mol/L | |
| B. | 溶液中的c(H+)为1×10-4mol/L | |
| C. | 溶液中由水电离出来的c(OH-)为1×10-10mol/L | |
| D. | 溶液中由水电离出来的H+的浓度为1×10-4mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com