

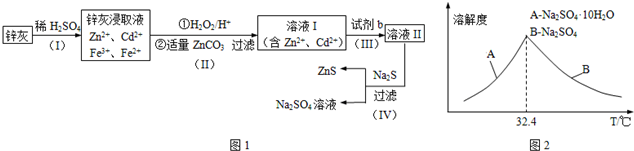
分析 根据实验原理,PbO与C反应生成CO和CO2,用澄清石灰水检验二氧化碳,由于CO有毒,为防止污染空气,所以要用醋酸二氨合铜吸收CO,吸收尾气,因为空气中有氧气,为防止氧气的干扰,要先用氮气氢装置中的空气排尽,
(1)在反应的开始,主要发生PbO+C $\frac{\underline{\;\;△\;\;}}{\;}$Pb+CO,CO不能使澄清石灰水变浑浊;
(2)CO有毒,会污染空气,据此分析;
(3)醋酸二氨合铜吸收CO的反应:〔Cu (NH3)2〕Ac+CO+NH3$\frac{\underline{\;\;△\;\;}}{\;}$〔Cu (NH3)3〕Ac•CO;△H<0,该反应为气体体积减小的放热的可逆反应,根据影响平衡移动因素分析问题;
解答 解:(1)在反应的开始,主要发生PbO+C $\frac{\underline{\;\;△\;\;}}{\;}$Pb+CO,生成的二氧化碳很少,CO不能使澄清石灰水变浑浊,
故答案为:开始主要是发生反应①,生成的二氧化碳很少;
(2)CO有毒,会污染空气,所以烧杯中醋酸二氨合铜 (〔Cu (NH3)2〕Ac ) 的作用为吸收一氧化碳,防止污染空气,
故答案为:吸收一氧化碳,防止污染空气;
(3)醋酸二氨合铜吸收CO的反应:〔Cu (NH3)2〕Ac+CO+NH3$\stackrel{△}{?}$〔Cu (NH3)3〕Ac•CO;△H<0,该反应为气体体积减小的放热反应,实验后的醋酸二氨合铜经适当处理又可再生,即要使该反应向逆反应方向移动,所以适宜于再生的生产条件是加热、降压,
故答案为:加热、降压.
点评 本题以氧化铅中氧元素的检验为载体,考查实验的基本操作和原理分析,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意实验原理的分析,难度不大.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
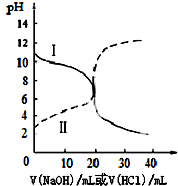 25℃时,取浓度均为0.1mol•L-1的醋酸溶液和氨水溶液各20mL,分别用浓度均为0.1mol•L-1NaOH溶液和盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法不正确的是( )
25℃时,取浓度均为0.1mol•L-1的醋酸溶液和氨水溶液各20mL,分别用浓度均为0.1mol•L-1NaOH溶液和盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法不正确的是( )| A. | 曲线Ⅰ:滴加溶液到20 mL时溶液的pH=5则:c(H+)-c((NH3•H2O)=c(OH-)=1×10-9 mol•L-1 | |
| B. | 曲线Ⅰ:滴加溶液到20 mL时:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| C. | 曲线Ⅱ:滴加溶液在10 mL~20 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+) | |
| D. | 曲线Ⅱ:滴加溶液到10 mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
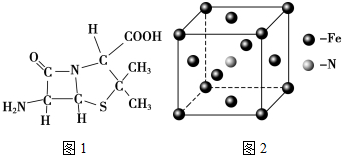
 )分子中有5n个σ键
)分子中有5n个σ键| 化学键 | Si-Si | O═O | Si-O |
| 键能(kJ•mol-1) | a | b | c |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.01mol/L CH3COOH溶液 | B. | 0.01mol/L HNO3溶液 | ||
| C. | pH=2的H2SO4溶液 | D. | pH=2的CH3COOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿矾一FeSO4•7H2O | B. | 芒硝一Na2SO4•10H2O | ||
| C. | 明矾一Al(SO4)3•12H2O | D. | 胆矾一CuSO4•5H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com